ცოდნა სინათლეა - Knowledge is light - Знание свет -
ქსოვილების ინჟინერია არის ბიოსამედიცინო ინჟინერიის დისციპლინა, რომელიც იყენებს უჯრედების , ინჟინერიის , მასალების მეთოდებისა და შესაფერისი ბიოქიმიური და ფიზიკურ-ქიმიური ფაქტორების კომბინაციას ბიოლოგიური ქსოვილების სხვადასხვა ტიპის აღსადგენად, შესანარჩუნებლად, გასაუმჯობესებლად ან ჩასანაცვლებლად . ქსოვილების ინჟინერია ხშირად გულისხმობს ქსოვილების ხარაჩოებზე განთავსებული უჯრედების გამოყენებას ახალი სიცოცხლისუნარიანი ქსოვილის სამედიცინო მიზნით ფორმირებისთვის, მაგრამ არ შემოიფარგლება მხოლოდ უჯრედებთან და ქსოვილების ხარაჩოებთან დაკავშირებული აპლიკაციებით. მიუხედავად იმისა, რომ ის ოდესღაც ბიომასალების ქვესფეროდ იყო კატეგორიზებული , მასშტაბისა და მნიშვნელობის ზრდის შემდეგ, ის შეიძლება ჩაითვალოს დამოუკიდებელ დარგად.
მიმოხილვა

ქსოვილის ინჟინერიის ფართოდ გავრცელებული განმარტება, როგორც ამას ლანგერი და ვაკანტი აცხადებენ , არის „ ინტერდისციპლინარული სფერო, რომელიც იყენებს ინჟინერიისა და სიცოცხლის შემსწავლელი მეცნიერებების პრინციპებს ბიოლოგიური შემცვლელების შემუშავების მიმართულებით, რომლებიც აღადგენენ, ინარჩუნებენ ან აუმჯობესებენ [ბიოლოგიური ქსოვილის] ფუნქციას ან მთელ ორგანოს“. გარდა ამისა, ლანგერი და ვაკანტი ასევე აცხადებენ, რომ არსებობს ქსოვილის ინჟინერიის სამი ძირითადი ტიპი: უჯრედები, ქსოვილის წარმომქმნელი ნივთიერებები და უჯრედები + მატრიცა მიდგომა (ხშირად მოიხსენიება, როგორც ხარაჩო). ქსოვილის ინჟინერია ასევე განისაზღვრება, როგორც „ქსოვილების ზრდის პრინციპების გაგება და მათი გამოყენება კლინიკური გამოყენებისთვის ფუნქციური ჩანაცვლებითი ქსოვილის წარმოებისთვის“. შემდგომი აღწერა ამბობს, რომ „ქსოვილის ინჟინერიის ძირითადი ვარაუდია, რომ სისტემის ბუნებრივი ბიოლოგიის გამოყენება უფრო მეტ წარმატებას მისცემს თერაპიული სტრატეგიების შემუშავებას, რომლებიც მიზნად ისახავს ქსოვილის ფუნქციის ჩანაცვლებას, აღდგენას, შენარჩუნებას ან გაუმჯობესებას“.
ქსოვილების ინჟინერიის მულტიდისციპლინურ სფეროში განვითარებულმა მოვლენებმა ქსოვილების შემცვლელი ნაწილებისა და დანერგვის სტრატეგიების ახალი ნაკრები მოგვცა. ბიომასალების , ღეროვანი უჯრედების, ზრდისა და დიფერენციაციის ფაქტორების და ბიომიმეტური გარემოს სამეცნიერო მიღწევებმა უნიკალური შესაძლებლობები შექმნა ლაბორატორიაში არსებული ქსოვილების შესაქმნელად ან გასაუმჯობესებლად ინჟინერიით შექმნილი უჯრედგარე მატრიცების („სკაფოლდები“), უჯრედებისა და ბიოლოგიურად აქტიური მოლეკულების კომბინაციებიდან. ქსოვილების ინჟინერიის წინაშე მდგარ მთავარ გამოწვევებს შორისაა უფრო რთული ფუნქციონალურობის, ბიომექანიკური სტაბილურობისა და ვასკულარიზაციის საჭიროება ლაბორატორიაში ტრანსპლანტაციისთვის განკუთვნილ ქსოვილებში.
ეტიმოლოგია
ტერმინის ისტორიული წარმოშობა გაურკვეველია, რადგან სიტყვის განმარტება ბოლო რამდენიმე ათწლეულის განმავლობაში შეიცვალა. ტერმინი პირველად 1984 წლის პუბლიკაციაში გამოჩნდა, რომელშიც აღწერილი იყო ენდოთელიუმის მსგავსი მემბრანის ორგანიზაცია გრძელ, სინთეზურ ოფთალმოლოგიურ პროთეზის ზედაპირზე.
ტერმინის პირველი თანამედროვე გამოყენება, როგორც დღეს არის აღიარებული, 1985 წელს მოხდა საინჟინრო კვლევითი ცენტრის მკვლევარის, ფიზიოლოგისა და ბიოინჟინერის, იუან-ჩენგ ფუნგის მიერ . მან შემოგვთავაზა ტერმინების „ქსოვილის“ (უჯრედებსა და ორგანოებს შორის ფუნდამენტური ურთიერთობის აღსანიშნავად) და „ინჟინერიის“ (აღნიშნული ქსოვილების მოდიფიკაციის სფეროს აღსანიშნავად) გაერთიანება. ტერმინი ოფიციალურად 1987 წელს იქნა მიღებული.
ისტორია
ანტიკური ხანა (მე-17 საუკუნემდე)
ადამიანის ქსოვილების შინაგანი ფუნქციონირების გაგება შესაძლოა გაცილებით უფრო ღრმად ითვლებოდეს, ვიდრე ბევრი მოელოდა. ჯერ კიდევ ნეოლითის პერიოდში გამოიყენებოდა ნაკერები ჭრილობების დასახურავად და შეხორცების ხელშესაწყობად. მოგვიანებით, ისეთმა საზოგადოებებმა, როგორიცაა ძველი ეგვიპტე, შეიმუშავეს ჭრილობების შესაკერად უკეთესი მასალები, როგორიცაა თეთრეულის ნაკერები. დაახლოებით ძვ.წ. 2500 წელს ძველ ინდოეთში კანის გადანერგვა შემუშავდა დუნდულოებიდან კანის მოჭრით და ყურის, ცხვირის ან ტუჩების ჭრილობებზე მიკერებით. ძველი ეგვიპტელები ხშირად გვამებიდან კანს ცოცხალ ადამიანებზე გადანერგავდნენ და ცდილობდნენ თაფლის გამოყენებას ანტიბიოტიკის სახით და ცხიმის გამოყენებას დამცავი ბარიერის სახით ინფექციის თავიდან ასაცილებლად. ჩვენი წელთაღრიცხვით I და II საუკუნეებში გალო-რომაელებმა შეიმუშავეს ჭედური რკინის იმპლანტები და სტომატოლოგიური იმპლანტები ძველ მაიას ტომებშიც იყო.
განმანათლებლობა (XVII-XIX საუკუნეები)
მიუხედავად იმისა, რომ ამ უძველეს საზოგადოებებს ჰქონდათ შემუშავებული ტექნიკა, რომელიც თავის დროზე გაცილებით წინ იყო, მათ მაინც არ გააჩნდათ მექანიკური გაგება იმის შესახებ, თუ როგორ რეაგირებდა სხეული ამ პროცედურებზე. ეს მექანიკური მიდგომა რენე დეკარტის მიერ შემუშავებული მეცნიერების ემპირიული მეთოდის განვითარებასთან ერთად გაჩნდა. სერ ისააკ ნიუტონმა სხეულის აღწერა, როგორც „ფიზიოქიმიური მანქანა“ დაიწყო და ამტკიცებდა, რომ დაავადება ამ მანქანის ავარია იყო.
მე-17 საუკუნეში რობერტ ჰუკმა აღმოაჩინა უჯრედი და ბენედიქტ დე სპინოზას წერილში წამოიჭრა ორგანიზმში მიმდინარე დინამიურ პროცესებს შორის ჰომეოსტაზის იდეა. მე-18 საუკუნეში აბრაამ ტრემბლის მიერ ჩატარებულმა ჰიდრაზე ჩატარებულმა ექსპერიმენტებმა უჯრედების რეგენერაციული შესაძლებლობების შესწავლა დაიწყო. მე-19 საუკუნეში სხვადასხვა ლითონების სხეულთან ურთიერთქმედების უკეთ გაგებამ განაპირობა უკეთესი ნაკერების შემუშავება და ძვლის ფიქსაციისთვის ხრახნიანი და ფირფიტის იმპლანტებისკენ გადასვლა. გარდა ამისა, 1800-იანი წლების შუა პერიოდში პირველად გამოითქვა ჰიპოთეზა, რომ უჯრედ-გარემოს ურთიერთქმედება და უჯრედების პროლიფერაცია სასიცოცხლოდ მნიშვნელოვანი იყო ქსოვილების რეგენერაციისთვის.
თანამედროვე ეპოქა (XX და XXI საუკუნეები)
დროისა და ტექნოლოგიების განვითარებასთან ერთად, მუდმივად საჭიროა ცვლილებების შეტანა მკვლევართა მიერ კვლევისადმი მიდგომებში. ქსოვილების ინჟინერია საუკუნეების განმავლობაში ვითარდებოდა. თავდაპირველად ადამიანები ნიმუშებს პირდაპირ ადამიანის ან ცხოველის გვამებიდან იყენებდნენ. ახლა ქსოვილების ინჟინრებს აქვთ შესაძლებლობა, ხელახლა შექმნან ორგანიზმში არსებული მრავალი ქსოვილი თანამედროვე ტექნიკის გამოყენებით, როგორიცაა მიკროფაბრიკაცია და სამგანზომილებიანი ბიობეჭდვა, ნატიურ ქსოვილოვან უჯრედებთან/ღეროვან უჯრედებთან ერთად. ამ მიღწევებმა მკვლევარებს საშუალება მისცა, გაცილებით ეფექტურად შეექმნათ ახალი ქსოვილები. მაგალითად, ეს ტექნიკა საშუალებას იძლევა უფრო მეტი პერსონალიზაციისა, რაც უზრუნველყოფს უკეთეს ბიოშეთავსებადობას, იმუნური პასუხის შემცირებას, უჯრედულ ინტეგრაციას და სიცოცხლის ხანგრძლივობას. ეჭვგარეშეა, რომ ეს ტექნიკა გააგრძელებს განვითარებას, რადგან ბოლო ათწლეულის განმავლობაში ვაგრძელებთ მიკროფაბრიკაციისა და ბიობეჭდვის ევოლუციას.
1960 წელს ვიხტერლე და ლიმი პირველები იყვნენ, ვინც გამოაქვეყნეს ექსპერიმენტები ბიოსამედიცინო გამოყენების ჰიდროგელების შესახებ, მათი კონტაქტური ლინზების კონსტრუქციაში გამოყენებით. ამ სფეროში მუშაობა ნელა განვითარდა მომდევნო ორი ათწლეულის განმავლობაში, მაგრამ მოგვიანებით დიდი პოპულარობა მოიპოვა, როდესაც ჰიდროგელები ხელახლა გამოიყენეს წამლების მიწოდებისთვის. 1984 წელს ჩარლზ ჰალმა შეიმუშავა ბიობეჭდვა Hewlett-Packard-ის ჭავლური პრინტერის მოწყობილობად გადაქცევით, რომელსაც შეეძლო უჯრედების 2-D ფორმატში ჩალაგება. სამგანზომილებიანი (3-D) ბეჭდვა დანამატური წარმოების სახეობაა, რომელმაც მას შემდეგ სხვადასხვა გამოყენება ჰპოვა სამედიცინო ინჟინერიაში, მისი მაღალი სიზუსტისა და ეფექტურობის გამო. ბიოლოგ ჯეიმს ტომპსონის მიერ 1998 წელს პირველი ადამიანის ღეროვანი უჯრედების ხაზების შემუშავებით, რასაც მოჰყვა პირველი ლაბორატორიაში გაზრდილი შინაგანი ორგანოების გადანერგვა 1999 წელს და პირველი ბიოპრინტერის შექმნით 2003 წელს მისურის უნივერსიტეტის მიერ, როდესაც მათ დაბეჭდეს სფეროიდები ხარაჩოების გარეშე, 3-D ბიობეჭდვა სამედიცინო სფეროში უფრო ტრადიციულად გამოიყენებოდა, ვიდრე ოდესმე. აქამდე მეცნიერებმა შეძლეს მინი ორგანოიდების და ჩიპებზე ორგანოების დაბეჭდვა , რამაც ადამიანის სხეულის ფუნქციების შესახებ პრაქტიკული ინფორმაცია მოგვცა. ფარმაცევტული კომპანიები ამ მოდელებს იყენებენ მედიკამენტების შესამოწმებლად, სანამ ცხოველებზე კვლევებზე გადავლენ. თუმცა, სრულად ფუნქციონალური და სტრუქტურულად მსგავსი ორგანო ჯერ არ დაბეჭდილა. იუტას უნივერსიტეტის გუნდმა, როგორც ამბობენ, ყურები დაბეჭდა და წარმატებით გადაუნერგა ბავშვებს, რომლებიც დეფექტებით დაიბადნენ, რის გამოც მათი ყურები ნაწილობრივ განვითარებული იყო.
დღეს ჰიდროგელები 3D ბიობეჭდვისთვის ბიომელანის სასურველ არჩევნად ითვლება, რადგან ისინი უჯრედების ბუნებრივ უჯრედშორისი უჯრედშორისი მატრიქსის (ECM) იმიტაციას ახდენენ და ამავდროულად, 3D სტრუქტურების შენარჩუნების უნარის მქონე ძლიერ მექანიკურ თვისებებსაც შეიცავს. გარდა ამისა, ჰიდროგელები 3D ბიობეჭდვასთან ერთად მკვლევრებს საშუალებას აძლევს შექმნან სხვადასხვა ხარაჩოები, რომელთა გამოყენებაც ახალი ქსოვილების ან ორგანოების ფორმირებისთვისაა შესაძლებელი. 3D დაბეჭდილი ქსოვილები კვლავ მრავალი გამოწვევის წინაშე დგანან, როგორიცაა სისხლძარღვოვანი სისტემის დამატება. ამასობაში, ქსოვილების ნაწილების 3D ბეჭდვა ნამდვილად გააუმჯობესებს ადამიანის სხეულის შესახებ ჩვენს გაგებას, რითაც დააჩქარებს როგორც საბაზისო, ასევე კლინიკურ კვლევებს.
მაგალითები

ლანგერისა და ვაკანტის განმარტებით, ქსოვილოვანი ინჟინერიის მაგალითები სამიდან ერთ ან რამდენიმე კატეგორიად იყოფა: „უბრალოდ უჯრედები“, „უჯრედები და ხარაჩო“ ან „ქსოვილის გამომწვევი ფაქტორები“.
- ინ ვიტრო ხორცი : საკვებად ვარგისი ხელოვნური ცხოველის კუნთოვანი ქსოვილი, რომელიც კულტივირებულია ინ ვიტრო პირობებში .
- ბიოხელოვნური ღვიძლის მოწყობილობა , „დროებითი ღვიძლი“, ექსტრაკორპორალური ღვიძლის დამხმარე მოწყობილობა (ELAD): ადამიანის ჰეპატოციტების უჯრედულ ხაზს (C3A ხაზი) ღრუ ბოჭკოვან ბიორეაქტორში შეუძლია ღვიძლის ღვიძლის ფუნქციის იმიტაცია ღვიძლის უკმარისობის მწვავე შემთხვევებისთვის. სრულად ქმედითი ELAD დროებით იფუნქციონირებს როგორც ინდივიდის ღვიძლი, რითაც თავიდან აიცილებს ტრანსპლანტაციას და საშუალებას მისცემს საკუთარი ღვიძლის რეგენერაციას.
- ხელოვნური პანკრეასი : კვლევა მოიცავს კუნძულოვანი უჯრედების გამოყენებას ორგანიზმში სისხლში შაქრის დონის რეგულირებისთვის, განსაკუთრებით დიაბეტის შემთხვევებში . ბიოქიმიური ფაქტორები შეიძლება გამოყენებულ იქნას ადამიანის პლურიპოტენტური ღეროვანი უჯრედების დიფერენცირების (გადაქცევის) უჯრედებად, რომლებიც ფუნქციონირებენ ბეტა უჯრედების მსგავსად , რომლებიც ინსულინის გამომუშავებაზე პასუხისმგებელ კუნძულოვან უჯრედშია .
- ხელოვნური შარდის ბუშტები : ენტონი ატალამ ( უეიკ ფორესტის უნივერსიტეტი ) წარმატებით ჩანერგა ხელოვნური შარდის ბუშტები, რომლებიც აგებულია კულტივირებული უჯრედებისგან, რომლებიც დათესილია შარდის ბუშტის ფორმის ხარაჩოზე, დაახლოებით 20 ადამიანიდან შვიდში, ხანგრძლივი ექსპერიმენტის ფარგლებში .
- ხრტილი : ლაბორატორიაში გაზრდილი ხრტილი, რომელიც in vitro კულტივირებული იყო ხარაჩოზე, წარმატებით გამოიყენეს აუტოლოგიური ტრანსპლანტაციის სახით პაციენტების მუხლების აღსადგენად.
- ხარაჩოს გარეშე ხრტილი: ხრტილი, რომელიც წარმოიქმნება ეგზოგენური ხარაჩოს მასალის გამოყენების გარეშე. ამ მეთოდოლოგიაში, კონსტრუქციაში შემავალი ყველა მასალა უჯრედულად წარმოიქმნება უშუალოდ უჯრედების მიერ.
- ბიოხელოვნური გული : დორის ტეილორის ლაბორატორიამ ბიოშეთავსებადი ვირთხის გული ააგო დეცელულარიზებული ვირთხის გულის რეცელულარიზაციით. ეს ხარაჩო და უჯრედები ბიორეაქტორში მოათავსეს , სადაც ის მომწიფდა და ნაწილობრივ ან სრულად გადანერგვადი ორგანო გახდა. ამ ნამუშევარს „ლანდმარკს“ უწოდებდნენ. ლაბორატორიამ თავდაპირველად ვირთხის გულიდან უჯრედები მოაშორა (პროცესი, რომელსაც „ დეცელულარიზაცია “ ეწოდება) და შემდეგ ვირთხის ღეროვანი უჯრედები დეცელულარიზებულ ვირთხის გულში შეიყვანეს.
- ქსოვილის ინჟინერიით შექმნილი სისხლძარღვები : ლაბორატორიაში გაზრდილი სისხლძარღვები, რომელთა გამოყენება შესაძლებელია დაზიანებული სისხლძარღვების აღსადგენად იმუნური პასუხის გამოწვევის გარეშე . ქსოვილის ინჟინერიით შექმნილი სისხლძარღვები შემუშავებულია მრავალი განსხვავებული მიდგომით. მათი იმპლანტაცია შესაძლებელია წინასწარ დათესილი უჯრედული სისხლძარღვების სახით, დეცელულარიზებული სისხლძარღვებით დამზადებული უჯრედული სისხლძარღვოვანი გრაფტების ან სინთეზური სისხლძარღვოვანი გრაფტების სახით .
- ხელოვნური კანი, რომელიც დამზადებულია ჰიდროგელში ჩასმული ადამიანის კანის უჯრედებისგან , მაგალითად, საბრძოლო ველის დამწვრობის აღსადგენად ბიო-დაბეჭდილი კონსტრუქციების შემთხვევაში.
- ხელოვნური ძვლის ტვინი : გადანერგვისთვის ინ ვიტრო კულტივირებული ძვლის ტვინი ქსოვილების ინჟინერიის „უბრალო უჯრედების“ მიდგომას წარმოადგენს.
- ქსოვილის ინჟინერიით შექმნილი ძვალი: სტრუქტურული მატრიცა შეიძლება შედგებოდეს ისეთი ლითონებისგან, როგორიცაა ტიტანი, სხვადასხვა დეგრადაციის სიჩქარის მქონე პოლიმერებისგან ან კერამიკის გარკვეული ტიპებისგან. მასალები ხშირად ირჩევა ოსტეობლასტების მოსაზიდად , რათა ხელი შეუწყონ ძვლის რეფორმირებას და ბიოლოგიური ფუნქციის აღდგენას. პროცესის დასაჩქარებლად შესაძლებელია სხვადასხვა ტიპის უჯრედების პირდაპირ დამატება მატრიცაში.
- ლაბორატორიაში გაზრდილი პენისი : კურდღლის პენისების დეცელულარიზებული ხარაჩოები ხელახლა უჯრედულიზირებული იქნა გლუვი კუნთებისა და ენდოთელური უჯრედებით. შემდეგ ორგანო გადანერგილი იქნა ცოცხალ კურდღლებში და ფუნქციონირებდა მშობლიური ორგანოს მსგავსად, რაც მიუთითებს გენიტალური ტრავმის სამკურნალოდ პოტენციალზე .
- პირის ღრუს ლორწოვანი გარსის ქსოვილოვანი ინჟინერია იყენებს უჯრედებისა და ხარაჩოს მიდგომას პირის ღრუს ლორწოვანი გარსის სამგანზომილებიანი სტრუქტურისა და ფუნქციის რეპლიკაციისთვის .
უჯრედები, როგორც საშენი ბლოკები

უჯრედები ქსოვილების ინჟინერიის მიდგომების წარმატების ერთ-ერთი მთავარი კომპონენტია. ქსოვილების ინჟინერია იყენებს უჯრედებს, როგორც ახალი ქსოვილის შექმნის/ჩანაცვლების სტრატეგიას. მაგალითებია ფიბრობლასტები, რომლებიც გამოიყენება კანის აღდგენის ან განახლებისთვის, ქონდროციტები, რომლებიც გამოიყენება ხრტილის აღდგენისთვის (MACI–FDA-ს მიერ დამტკიცებული პროდუქტი) და ჰეპატოციტები, რომლებიც გამოიყენება ღვიძლის დამხმარე სისტემებში .
ქსოვილების ინჟინერიის აპლიკაციებისთვის უჯრედების გამოყენება შესაძლებელია როგორც დამოუკიდებლად, ასევე დამხმარე მატრიცებთან ერთად. უჯრედების ზრდის, დიფერენციაციისა და არსებულ ქსოვილთან ინტეგრაციის ხელშეწყობის ადეკვატური გარემო უჯრედებზე დაფუძნებული საშენი ბლოკებისთვის კრიტიკული ფაქტორია. ამ უჯრედული პროცესებიდან ნებისმიერის მანიპულირება ახალი ქსოვილის განვითარების ალტერნატიულ გზებს ქმნის (მაგ., უჯრედების რეპროგრამირება - სომატური უჯრედები, ვასკულარიზაცია).
Იზოლაცია
უჯრედების იზოლაციის ტექნიკა დამოკიდებულია უჯრედის წყაროზე. ცენტრიფუგირება და აფერეზი არის მეთოდები, რომლებიც გამოიყენება უჯრედების ბიოსითხეებიდან (მაგ., სისხლიდან) ამოსაღებად. მაშინ როდესაც ქსოვილებიდან/ორგანოებიდან უჯრედების ამოსაღებად ცენტრიფუგირების ან აფერეზის ტექნიკის გამოყენებამდე საჭიროა მონელების პროცესები, რომლებიც ჩვეულებრივ იყენებენ ფერმენტებს უჯრედგარე მატრიქსის (ECM) მოსაშორებლად. ტრიფსინი და კოლაგენაზა ყველაზე გავრცელებული ფერმენტებია, რომლებიც გამოიყენება ქსოვილების მონელებისთვის. მიუხედავად იმისა, რომ ტრიფსინი ტემპერატურაზეა დამოკიდებული, კოლაგენაზა ნაკლებად მგრძნობიარეა ტემპერატურის ცვლილებების მიმართ.
ფიჭური წყაროები
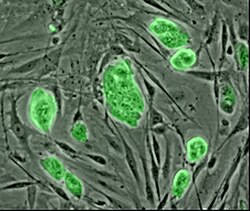
პირველადი უჯრედები არის ის უჯრედები, რომლებიც პირდაპირ იზოლირებულია მასპინძელი ქსოვილისგან. ეს უჯრედები უზრუნველყოფენ უჯრედის ქცევის ექს ვივო მოდელს ყოველგვარი გენეტიკური, ეპიგენეტიკური ან განვითარების ცვლილებების გარეშე, რაც მათ უფრო მეტად რეპლიკაციას უკეთებს ინ ვივო პირობებში, ვიდრე სხვა მეთოდებით მიღებული უჯრედები. თუმცა, ამ შეზღუდვამ შეიძლება გაართულოს მათი შესწავლა. ეს არის მომწიფებული უჯრედები, ხშირად ტერმინალურად დიფერენცირებული, რაც ნიშნავს, რომ მრავალი ტიპის უჯრედისთვის პროლიფერაცია რთულია ან შეუძლებელია. გარდა ამისა, მიკროგარემოსი, რომელშიც ეს უჯრედები არსებობს, მაღალ სპეციალიზებულია, რაც ხშირად ართულებს ამ პირობების რეპლიკაციას.
მეორადი უჯრედები პირველადი კულტურიდან უჯრედების ნაწილი გადადის ახალ საცავში/ჭურჭელში კულტივირების გასაგრძელებლად. პირველადი კულტურიდან ამოღებულია გარემო, მიიღება გადასატანი სასურველი უჯრედები და შემდეგ კულტივირდება ახალ ჭურჭელში ახალი ზრდის გარემოთი. მეორადი უჯრედული კულტურა სასარგებლოა იმის უზრუნველსაყოფად, რომ უჯრედებს ჰქონდეთ როგორც სივრცე, ასევე საკვები ნივთიერებები, რომლებიც მათ ზრდისთვის სჭირდებათ. მეორადი კულტურები განსაკუთრებით გამოიყენება ნებისმიერ სცენარში, როდესაც სასურველია უჯრედების უფრო დიდი რაოდენობა, ვიდრე პირველად კულტურაშია ნაპოვნი. მეორადი უჯრედები იზიარებენ პირველადი უჯრედების შეზღუდვებს (იხილეთ ზემოთ), მაგრამ ახალ ჭურჭელში გადატანისას მათ აქვთ დაბინძურების დამატებითი რისკი.
უჯრედების გენეტიკური კლასიფიკაცია
აუტოლოგიური: უჯრედების დონორი და მიმღები ერთი და იგივე ინდივიდია. უჯრედები გროვდება, კულტივირდება ან ინახება და შემდეგ ხელახლა ეძლევა მასპინძელს. მასპინძლის საკუთარი უჯრედების ხელახლა შეყვანის შედეგად, ანტიგენური პასუხი არ წარმოიქმნება. ორგანიზმის იმუნური სისტემა ამ ხელახლა იმპლანტირებულ უჯრედებს საკუთარ უჯრედებად ცნობს და არ ისახავს მიზნად მათ შეტევისთვის. აუტოლოგიური უჯრედების დამოკიდებულება მასპინძელი უჯრედების ჯანმრთელობასა და დონორის ადგილის ავადობაზე შეიძლება მათი გამოყენების შემაფერხებელი ფაქტორი იყოს. ცხიმოვანი და ძვლის ტვინიდან მიღებული მეზენქიმური ღეროვანი უჯრედები, როგორც წესი, აუტოლოგიური ხასიათისაა და მათი გამოყენება მრავალი გზით შეიძლება, ჩონჩხის ქსოვილის აღდგენის ხელშეწყობიდან დაწყებული, დიაბეტით დაავადებულ პაციენტებში ბეტა უჯრედების შევსებით დამთავრებული.
ალოგენური: უჯრედები მიიღება იმავე სახეობის დონორის სხეულიდან, რომელიც რეციპიენტია. მიუხედავად იმისა, რომ ადამიანის უჯრედების გამოყენებას in vitro კვლევებისთვის (მაგალითად, ადამიანის ტვინის ქსოვილის ქიმერას განვითარება ) გარკვეული ეთიკური შეზღუდვები აქვს, ადამიანის ჩუჩადან კანის ფიბრობლასტების გამოყენება იმუნოლოგიურად უსაფრთხო და შესაბამისად, კანის ალოგენური ქსოვილის ინჟინერიისთვის სიცოცხლისუნარიან არჩევანს წარმოადგენს.
ქსენოგენური: ეს უჯრედები რეციპიენტის ალტერნატიული სახეობებიდან მიღებული იზოლირებული უჯრედებია. ქსენოგენური ქსოვილის გამოყენების აღსანიშნავი მაგალითია გულ-სისხლძარღვთა იმპლანტების კონსტრუქცია ცხოველური უჯრედების მეშვეობით. ქიმერული ადამიანი-ცხოველის მეურნეობა ეთიკურ შეშფოთებას იწვევს ცხოველებში ადამიანის ორგანოების იმპლანტაციით ცნობიერების გაუმჯობესების პოტენციალთან დაკავშირებით.
სინგენური ან იზოგენური: ეს უჯრედები აღწერს იდენტური გენეტიკური კოდიდან წარმოქმნილ უჯრედებს. ეს ანიჭებს აუტოლოგიური უჯრედული ხაზების მსგავს იმუნოლოგიურ სარგებელს (იხ. ზემოთ). აუტოლოგიური უჯრედები შეიძლება ჩაითვალოს სინგენურად, მაგრამ კლასიფიკაცია ასევე ვრცელდება არააუტოლოგურად მიღებულ უჯრედებზე, როგორიცაა იდენტური ტყუპებისგან, გენეტიკურად იდენტური (კლონირებული) კვლევითი მოდელებიდან ან ინდუცირებული ღეროვანი უჯრედებიდან (iSC) , დონორთან დაკავშირებული უჯრედების მიხედვით.
ღეროვანი უჯრედები
ღეროვანი უჯრედები არადიფერენცირებული უჯრედებია, რომლებსაც კულტურაში დაყოფის და სპეციალიზებული უჯრედების სხვადასხვა ფორმის წარმოქმნის უნარი აქვთ. ღეროვანი უჯრედები წყაროს მიხედვით იყოფა „ზრდასრულ“ და „ემბრიონულ“ ღეროვან უჯრედებად. მიუხედავად იმისა, რომ ემბრიონული ღეროვანი უჯრედების გამოყენებასთან დაკავშირებით ჯერ კიდევ დიდი ეთიკური დებატები მიმდინარეობს, ითვლება, რომ კიდევ ერთი ალტერნატიული წყარო - ინდუცირებული პლურიპოტენტური ღეროვანი უჯრედები - შეიძლება სასარგებლო იყოს დაავადებული ან დაზიანებული ქსოვილების აღსადგენად ან შეიძლება გამოყენებულ იქნას ახალი ორგანოების გასაზრდელად.
ტოტიპოტენტური უჯრედები არის ღეროვანი უჯრედები, რომლებსაც შეუძლიათ დაყოფა შემდგომ ღეროვან უჯრედებად ან დიფერენცირება ორგანიზმში ნებისმიერი ტიპის უჯრედად, მათ შორის ექსტრაემბრიონულ ქსოვილად.
პლურიპოტენტური უჯრედები ღეროვანი უჯრედებია, რომლებსაც შეუძლიათ ორგანიზმში ნებისმიერი ტიპის უჯრედად დიფერენცირება, გარდა ექსტრაემბრიონული ქსოვილისა. ინდუცირებული პლურიპოტენტური ღეროვანი უჯრედები (iPSCs) პლურიპოტენტური ღეროვანი უჯრედების ქვეკლასია, რომლებიც ემბრიონულ ღეროვან უჯრედებს (ESCs) წააგავს და რომლებიც ზრდასრული დიფერენცირებული უჯრედებიდან არის მიღებული. iPSCs იქმნება ზრდასრულ უჯრედებში ტრანსკრიფციული ფაქტორების ექსპრესიის შეცვლით მანამ, სანამ ისინი ემბრიონულ ღეროვან უჯრედებს არ დაემსგავსებიან.
მულტიპოტენტური ღეროვანი უჯრედების დიფერენცირება შესაძლებელია იმავე კლასის ნებისმიერ უჯრედად, მაგალითად, სისხლის ან ძვლის უჯრედებად . მულტიპოტენტური უჯრედების გავრცელებული მაგალითია მეზენქიმური ღეროვანი უჯრედები (MSCs).
ხარაჩოები
ხარაჩოები არის მასალები, რომლებიც შექმნილია სასურველი უჯრედული ურთიერთქმედებების გამოსაწვევად, რათა ხელი შეუწყონ ახალი ფუნქციური ქსოვილების ფორმირებას სამედიცინო მიზნებისთვის. უჯრედები ხშირად „ითესება“ ამ სტრუქტურებში, რომლებსაც შეუძლიათ სამგანზომილებიანი ქსოვილის ფორმირების მხარდაჭერა. ხარაჩოები ბაძავენ მშობლიური ქსოვილის უჯრედგარე მატრიქსს, იმეორებენ in vivo გარემოს და საშუალებას აძლევენ უჯრედებს, გავლენა მოახდინონ საკუთარ მიკროგარემოსზე. ისინი, როგორც წესი, ემსახურებიან შემდეგი მიზნებიდან სულ მცირე ერთს: უჯრედების მიმაგრებისა და მიგრაციის უზრუნველყოფას, უჯრედებისა და ბიოქიმიური ფაქტორების მიწოდებასა და შენარჩუნებას, უჯრედებისთვის სასიცოცხლო საკვები ნივთიერებებისა და ექსპრესირებული პროდუქტების დიფუზიის უზრუნველყოფას და გარკვეული მექანიკური და ბიოლოგიური გავლენის მოხდენას უჯრედული ფაზის ქცევის შესაცვლელად.
2009 წელს, თორაკალური ქირურგის, ტორსტენ უოლესის ხელმძღვანელობით, ინტერდისციპლინურმა გუნდმა წარმატებით ჩაუტარა პაციენტს, რომელიც ტრაქეის რეკონსტრუქციას ელოდა, პირველი ბიოხელოვნური ტრანსპლანტატი, რომელიც ტრანსპლანტაციის შემდგომი ტრანსპლანტაციისთვის თანდაყოლილ სისხლძარღვოვან ქსელს უზრუნველყოფს, წარმატებით.
ქსოვილების რეკონსტრუქციის მიზნის მისაღწევად, ხარაჩოები უნდა აკმაყოფილებდეს გარკვეულ სპეციფიკურ მოთხოვნებს. მაღალი ფორიანობა და ფორების საკმარისი ზომა აუცილებელია უჯრედების დათესვისა და დიფუზიის ხელშესაწყობად, როგორც უჯრედების, ასევე საკვები ნივთიერებების მთელ სტრუქტურაში. ბიოდეგრადირება ხშირად აუცილებელი ფაქტორია, რადგან ხარაჩოები სასურველია შეიწოვოს მიმდებარე ქსოვილებმა ქირურგიული მოცილების საჭიროების გარეშე. დეგრადაციის სიჩქარე მაქსიმალურად უნდა ემთხვეოდეს ქსოვილის ფორმირების სიჩქარეს: ეს ნიშნავს, რომ სანამ უჯრედები საკუთარ ბუნებრივ მატრიცულ სტრუქტურას ქმნიან საკუთარ გარშემო, ხარაჩოს შეუძლია უზრუნველყოს სტრუქტურული მთლიანობა სხეულში და საბოლოოდ ის დაიშლება, რის შედეგადაც ახლად წარმოქმნილი ქსოვილი დარჩება, რომელიც მექანიკურ დატვირთვას აიღებს. ინექციურობა ასევე მნიშვნელოვანია კლინიკური გამოყენებისთვის. ორგანოების ბეჭდვის ბოლოდროინდელი კვლევები აჩვენებს, თუ რამდენად მნიშვნელოვანია 3D გარემოს კარგი კონტროლი ექსპერიმენტების რეპროდუცირების უზრუნველსაყოფად და უკეთესი შედეგების შესათავაზებლად.
მასალები
მასალის შერჩევა ხარაჩოს დამზადების აუცილებელი ასპექტია. გამოყენებული მასალები შეიძლება იყოს ბუნებრივი ან სინთეტიკური და შეიძლება იყოს ბიოდეგრადირებადი ან არაბიოდეგრადირებადი. გარდა ამისა, ისინი უნდა იყვნენ ბიოშეთავსებადი, რაც იმას ნიშნავს, რომ ისინი არ იწვევენ რაიმე უარყოფით გავლენას უჯრედებზე. მაგალითად, სილიკონი არის სინთეტიკური, არაბიოდეგრადირებადი მასალა, რომელიც ხშირად გამოიყენება წამლის მიწოდების მასალად, ხოლო ჟელატინი არის ბიოდეგრადირებადი, ბუნებრივი მასალა, რომელიც ხშირად გამოიყენება უჯრედული კულტურების ხარაჩოებში
თითოეული გამოყენებისთვის საჭირო მასალა განსხვავებულია და დამოკიდებულია მასალის სასურველ მექანიკურ თვისებებზე. მაგალითად, გრძელი ძვლების დეფექტების ქსოვილოვანი ინჟინერიისთვის საჭიროა ხისტი ხარაჩო, რომლის შეკუმშვის სიმტკიცე კორტიკალური ძვლის მსგავსია (100-150 მპა), რაც გაცილებით მაღალია კანის რეგენერაციის ხარაჩოსთან შედარებით.
არსებობს რამდენიმე მრავალმხრივი სინთეზური მასალა, რომლებიც გამოიყენება ხარაჩოების სხვადასხვა გამოყენებისთვის. ერთ-ერთი ასეთი ხშირად გამოყენებული მასალაა პოლირძემჟავა (PLA), სინთეზური პოლიმერი. PLA - პოლირძემჟავა. ეს არის პოლიესტერი, რომელიც ადამიანის ორგანიზმში იშლება რძემჟავას წარმოქმნით , ბუნებრივად წარმოქმნილი ქიმიური ნივთიერება, რომელიც ადვილად გამოიყოფა ორგანიზმიდან. მსგავსი მასალებია პოლიგლიკოლის მჟავა (PGA) და პოლიკაპროლაქტონი (PCL): მათი დაშლის მექანიზმი PLA-ს მსგავსია, მაგრამ PCL ნელა იშლება და PGA უფრო სწრაფად. PLA ხშირად ერწყმის PGA-ს პოლი-რძემჟავა-კო-გლიკოლის მჟავას (PLGA) შესაქმნელად. ეს განსაკუთრებით სასარგებლოა, რადგან PLGA-ს დაშლის მორგება შესაძლებელია PLA-სა და PGA-ს წონითი პროცენტული მაჩვენებლების შეცვლით: მეტი PLA - ნელა დეგრადაცია, მეტი PGA - უფრო სწრაფი დეგრადაცია. ეს მორგება, მის ბიოშეთავსებადობასთან ერთად, მას ხარაჩოების შესაქმნელად უაღრესად სასარგებლო მასალად აქცევს.
ხარაჩოები ასევე შეიძლება დამზადდეს ბუნებრივი მასალებისგან: კერძოდ, შესწავლილია უჯრედგარე მატრიქსის სხვადასხვა წარმოებულები, რათა შეფასდეს მათი უნარი, ხელი შეუწყონ უჯრედების ზრდას. ცილაზე დაფუძნებული მასალები - როგორიცაა კოლაგენი ან ფიბრინი , და პოლისაქარიდური მასალები - როგორიცაა ქიტოზანი ან გლიკოზამინოგლიკანები (GAGs), ყველა შესაფერისი აღმოჩნდა უჯრედების თავსებადობის თვალსაზრისით. GAG-ებს შორის, ჰიალურონის მჟავა , შესაძლოა ჯვარედინი შემაკავშირებელ აგენტებთან (მაგ., გლუტარალდეჰიდი , წყალში ხსნადი კარბოდიიმიდი და ა.შ.) კომბინაციაში , ხარაჩოს მასალის ერთ-ერთი შესაძლო არჩევანია. თიოლის ჯგუფების ამ პოლიმერებთან კოვალენტური მიმაგრების გამო, მათ შეუძლიათ ჯვარედინი შეერთება დისულფიდური ბმების წარმოქმნით. [თიოლირებული პოლიმერების ( თიომერების ) გამოყენება ქსოვილების ინჟინერიისთვის ხარაჩოს მასალად პირველად 2001 წელს , ვენაში , ფარმაცევტული ტექნოლოგიების მე-4 ცენტრალური ევროპის სიმპოზიუმზე იქნა წარმოდგენილი. რადგან თიომერები ბიოშეთავსებადია, ავლენენ უჯრედების მიმბაძველ თვისებებს და ეფექტურად უჭერენ მხარს სხვადასხვა ტიპის უჯრედების პროლიფერაციას და დიფერენციაციას, ისინი ფართოდ გამოიყენება ქსოვილების ინჟინერიისთვის ხარაჩოებად. გარდა ამისა, თიომერები, როგორიცაა თიოლირებული ჰიალურონის მჟავა და თიოლირებული ქიტოზანი , ავლენენ ჭრილობების შეხორცების თვისებებს და მრავალი კლინიკური კვლევის საგანია . გარდა ამისა, უჯრედგარე მატრიქსის ცილის ფრაგმენტი, როგორიცაა RGD პეპტიდი , შეიძლება დაუკავშირდეს არაბიოაქტიურ მასალას უჯრედების მიმაგრების ხელშესაწყობად. ხარაჩოს კიდევ ერთი ფორმაა დეცელულარიზებული ქსოვილი. ეს არის პროცესი, სადაც ქიმიკატები გამოიყენება უჯრედების ქსოვილებიდან ამოსაღებად, მხოლოდ უჯრედგარე მატრიცა რჩება. ამას აქვს სრულად ჩამოყალიბებული მატრიცა, რომელიც სპეციფიკურია სასურველი ქსოვილის ტიპისთვის. თუმცა, დეცელულირებულმა ხარაჩომ შესაძლოა იმუნური პრობლემები შექმნას მომავალში შეყვანილი უჯრედების შემთხვევაში.
სინთეზი
ლიტერატურაში აღწერილია ქსოვილოვანი ინჟინერიის ხარაჩოებად გამოსაყენებელი ფოროვანი სტრუქტურების მომზადების მრავალი განსხვავებული მეთოდი. თითოეულ ამ ტექნიკას თავისი უპირატესობები აქვს, მაგრამ არცერთი არ არის ნაკლოვანებების გარეშე.
ნანოფიბრის თვითშეკრება
მოლეკულური თვითაწყობა ერთ-ერთი იმ მცირერიცხოვან მეთოდთაგანია ბიომასალების შესაქმნელად, რომელთა თვისებები მასშტაბითა და ქიმიით მსგავსია ბუნებრივი in vivo უჯრედგარე მატრიქსის (ECM), რაც რთული ქსოვილების ქსოვილოვანი ინჟინერიისკენ გადადგმულ გადამწყვეტ ნაბიჯს წარმოადგენს. გარდა ამისა, ამ ჰიდროგელის ხარაჩოებმა აჩვენა უპირატესობა in vivo ტოქსიკოლოგიასა და ბიოშეთავსებადობაში ტრადიციულ მაკრო-ხარაჩოებთან და ცხოველური წარმოშობის მასალებთან შედარებით.
ტექსტილის ტექნოლოგიები
ეს ტექნიკა მოიცავს ყველა იმ მიდგომას, რომელიც წარმატებით იქნა გამოყენებული სხვადასხვა პოლიმერებისგან დამზადებული უქსოვი ბადეების დასამზადებლად . კერძოდ, უქსოვი პოლიგლიკოლიდური სტრუქტურები გამოიცადა ქსოვილების ინჟინერიის აპლიკაციებისთვის: ასეთი ბოჭკოვანი სტრუქტურები სასარგებლო აღმოჩნდა სხვადასხვა ტიპის უჯრედების გასაზრდელად. ძირითადი ნაკლოვანებები დაკავშირებულია მაღალი ფორიანობისა და რეგულარული ფორების ზომის მიღების სირთულეებთან.
გამხსნელის ჩამოსხმა და ნაწილაკების გამორეცხვა
გამხსნელით ჩამოსხმა და ნაწილაკების გამორეცხვა (SCPL) საშუალებას იძლევა მომზადდეს სტრუქტურები რეგულარული ფორიანობით, მაგრამ შეზღუდული სისქით. პირველ რიგში, პოლიმერი იხსნება შესაფერის ორგანულ გამხსნელში (მაგ., პოლირძემჟავა შეიძლება გაიხსნას დიქლორმეთანში ), შემდეგ ხსნარი იხსნება ფოროგენის ნაწილაკებით სავსე ყალიბში. ასეთი ფოროგენი შეიძლება იყოს არაორგანული მარილი, როგორიცაა ნატრიუმის ქლორიდი , საქაროზის კრისტალები , ჟელატინის სფეროები ან პარაფინის სფეროები. ფოროგენის ნაწილაკების ზომა გავლენას ახდენს ხარაჩოს ფორების ზომაზე, ხოლო პოლიმერისა და ფოროგენის თანაფარდობა პირდაპირ კორელაციაშია საბოლოო სტრუქტურის ფორიანობის რაოდენობასთან. პოლიმერული ხსნარის ჩამოსხმის შემდეგ, გამხსნელს აორთქლების საშუალება ეძლევა, შემდეგ ყალიბში არსებული კომპოზიტური სტრუქტურა იძირება ფოროგენის გახსნისთვის შესაფერისი სითხის აბაზანაში: წყალი ნატრიუმის ქლორიდის, საქაროზის და ჟელატინის შემთხვევაში ან ალიფატური გამხსნელი, როგორიცაა ჰექსანი პარაფინთან გამოსაყენებლად. ფოროგენის სრულად გახსნის შემდეგ მიიღება ფოროვანი სტრუქტურა. მცირე სისქის დიაპაზონის გარდა, SCPL-ის კიდევ ერთი ნაკლი ორგანული გამხსნელების გამოყენებაა, რომლებიც სრულად უნდა მოიხსნას ხარაჩოზე დათესილი უჯრედების შესაძლო დაზიანების თავიდან ასაცილებლად.
გაზის ქაფი
ორგანული გამხსნელებისა და მყარი პოროგენების გამოყენების საჭიროების დასაძლევად, შემუშავდა ტექნიკა, რომელიც იყენებს გაზს, როგორც პოროგენს. პირველ რიგში, სასურველი პოლიმერისგან დამზადებული დისკოს ფორმის სტრუქტურები მზადდება გაცხელებული ყალიბის გამოყენებით შეკუმშვის გზით. შემდეგ დისკები თავსდება კამერაში, სადაც ისინი რამდენიმე დღის განმავლობაში მაღალი წნევის CO2-ის ზემოქმედების ქვეშ იმყოფებიან . კამერაში წნევა თანდათან აღდგება ატმოსფერულ დონემდე. ამ პროცედურის დროს ფორები წარმოიქმნება პოლიმერის მიერ გამოყოფილი ნახშირორჟანგის მოლეკულებით, რაც იწვევს ღრუბლისებრ სტრუქტურას. ასეთი ტექნიკით გამოწვეული ძირითადი პრობლემები გამოწვეულია შეკუმშვის დროს გამოყენებული ჭარბი სითბოთი (რაც ხელს უშლის ნებისმიერი ტემპერატურისადმი არასტაბილური მასალის პოლიმერულ მატრიცაში შეტანას) და იმით, რომ ფორები არ ქმნიან ურთიერთდაკავშირებულ სტრუქტურას.
ემულსიფიკაცია, გაყინვა-გაშრობა
ეს ტექნიკა არ საჭიროებს მყარი პოროგენის, მაგალითად SCPL-ის გამოყენებას. პირველ რიგში, სინთეზური პოლიმერი იხსნება შესაფერის გამხსნელში (მაგ., პოლირძემჟავა დიქლორმეთანში), შემდეგ პოლიმერულ ხსნარს ემატება წყალი და ორი სითხე შერეულია ემულსიის მისაღებად . სანამ ორი ფაზა გამოეყოფა, ემულსია ისხდება ყალიბში და სწრაფად იყინება თხევად აზოტში ჩაძირვით . გაყინული ემულსია შემდგომში იყინება დისპერსიული წყლისა და გამხსნელის მოსაშორებლად, რითაც რჩება გამაგრებული, ფოროვანი პოლიმერული სტრუქტურა. მიუხედავად იმისა, რომ ემულსიფიკაცია და გაყინვით გაშრობა საშუალებას იძლევა უფრო სწრაფად მომზადდეს SCPL-თან შედარებით (რადგან ის არ საჭიროებს დროის ხარჯვას გამორეცხვის ეტაპზე), ის მაინც მოითხოვს გამხსნელების გამოყენებას. გარდა ამისა, ფორების ზომა შედარებით მცირეა და ფორიანობა ხშირად არარეგულარულია. გაყინვით გაშრობა თავისთავად ასევე ხშირად გამოყენებული ტექნიკაა ხარაჩოების დასამზადებლად. კერძოდ, იგი გამოიყენება კოლაგენის ღრუბლების დასამზადებლად: კოლაგენი იხსნება ძმარმჟავას ან მარილმჟავას მჟავე ხსნარებში , რომლებიც ისხდება ყალიბში, იყინება თხევადი აზოტით და შემდეგ ლიოფილიზდება .
თერმულად ინდუცირებული ფაზური გამოყოფა
წინა ტექნიკის მსგავსად, TIPS ფაზური გამოყოფის პროცედურა მოითხოვს დაბალი დნობის წერტილის მქონე გამხსნელის გამოყენებას, რომლის სუბლიმირებაც მარტივია. მაგალითად, დიოქსანის გამოყენება შესაძლებელია პოლირძემჟავას გასახსნელად, შემდეგ ფაზური გამოყოფა ხდება წყლის მცირე რაოდენობის დამატებით: წარმოიქმნება პოლიმერით მდიდარი და პოლიმერით ღარიბი ფაზები. გამხსნელის დნობის წერტილზე დაბლა გაგრილების და გამხსნელის სუბლიმაციისთვის ვაკუუმში გაშრობის რამდენიმე დღის შემდეგ, მიიღება ფოროვანი სტრუქტურა. სითხე-თხევადი ფაზური გამოყოფა ემულსიფიკაციის/გაყინვით გაშრობის იგივე ნაკლოვანებებს წარმოადგენს.
ელექტრო დატრიალება
ელექტროდაწნვა მრავალმხრივი ტექნიკაა, რომლის გამოყენება შესაძლებელია რამდენიმე მიკრონიდან რამდენიმე ნანომეტრამდე დიამეტრის უწყვეტი ბოჭკოების მისაღებად. ელექტროდაწნვის ტიპურ სისტემაში სასურველი ხარაჩოს მასალა იხსნება გამხსნელში და თავსდება შპრიცში. ეს ხსნარი მიეწოდება ნემსის მეშვეობით და მაღალი ძაბვა მიეწოდება წვერსა და გამტარ შემგროვებელ ზედაპირს. ხსნარში ელექტროსტატიკური ძალების დაგროვება იწვევს თხელი ბოჭკოვანი ნაკადის გამოტყორცნას საპირისპიროდ დამუხტული ან დამიწებული შემგროვებელი ზედაპირისკენ. ამ პროცესის დროს გამხსნელი აორთქლდება, რის შედეგადაც მყარი ბოჭკოები ტოვებს მაღალფოროვან ქსელს. ეს ტექნიკა ადვილად რეგულირებადია, გამხსნელის, ძაბვის, სამუშაო მანძილის (ნემსიდან შეგროვების ზედაპირამდე მანძილი), ხსნარის ნაკადის სიჩქარის, გახსნილი ნივთიერების კონცენტრაციის და შემგროვებელი ზედაპირის ვარიაციით. ეს საშუალებას იძლევა ბოჭკოების მორფოლოგიის ზუსტი კონტროლის.
კომერციულ დონეზე კი, მასშტაბირების მიზნით, ერთდროულად 40 ან ზოგჯერ 96 ნემსი მუშაობს. ასეთ მოწყობაში არსებული შემაფერხებელი ფაქტორებია: 1) ყველა ნემსისთვის ზემოაღნიშნული ცვლადების ერთგვაროვანი შენარჩუნება და 2) ცალკეულ ბოჭკოებში „მძივების“ წარმოქმნა, რომელთა დიამეტრიც ჩვენ, როგორც ინჟინრებს, გვსურს, ერთგვაროვანი იყოს. ისეთი ცვლადების შეცვლით, როგორიცაა კოლექტორამდე მანძილი, გამოყენებული ძაბვის სიდიდე ან ხსნარის ნაკადის სიჩქარე, მკვლევარებს შეუძლიათ მკვეთრად შეცვალონ ხარაჩოს საერთო არქიტექტურა.
ისტორიულად, ელექტროდწნული ბოჭკოვანი ხარაჩოების კვლევა, სულ მცირე, 1980-იანი წლების ბოლოთი თარიღდება, როდესაც საიმონმა აჩვენა, რომ ელექტროდწნული მეთოდით შესაძლებელია ნანო- და სუბმიკრონული მასშტაბის ბოჭკოვანი ხარაჩოების წარმოება პოლიმერული ხსნარებიდან, რომლებიც სპეციალურად განკუთვნილია უჯრედებისა და ქსოვილების სუბსტრატებად in vitro . ელექტროდწნული ბადეების უჯრედების კულტურისა და ქსოვილების ინჟინერიისთვის ადრეულმა გამოყენებამ აჩვენა, რომ სხვადასხვა ტიპის უჯრედები ეკვრის და მრავლდება პოლიკარბონატის ბოჭკოებზე. აღინიშნა, რომ 2D კულტურაში ტიპიურად დაფიქსირებული გაბრტყელებული მორფოლოგიისგან განსხვავებით, ელექტროდწნულ ბოჭკოებზე გაზრდილმა უჯრედებმა აჩვენეს უფრო მომრგვალებული, სამგანზომილებიანი მორფოლოგია, რომელიც ზოგადად შეინიშნება ქსოვილებში in vivo პირობებში .
CAD/CAM ტექნოლოგიები
რადგან ზემოთ ჩამოთვლილი ტექნიკების უმეტესობა შეზღუდულია ფორიანობისა და ფორების ზომის კონტროლის თვალსაზრისით, ქსოვილების ინჟინერიაში დანერგილია კომპიუტერული დიზაინისა და წარმოების ტექნიკა. პირველ რიგში, სამგანზომილებიანი სტრუქტურა იქმნება CAD პროგრამული უზრუნველყოფის გამოყენებით. ფორიანობის მორგება შესაძლებელია პროგრამულ უზრუნველყოფაში არსებული ალგორითმების გამოყენებით. შემდეგ ხარაჩო იქმნება პოლიმერული ფხვნილების ჭავლური ბეჭდვის ან პოლიმერული დნობის შედუღებული დეპონირების მოდელირების გამოყენებით .
ელ-აიუბის და სხვების მიერ 2011 წელს ჩატარებულმა კვლევამ გამოიკვლია „3D გრაფიკის ტექნიკა ( ბიოშეთავსებადი და ბიოდეგრადირებადი ) პოლი-L-ლაქტიდის მაკროფოროვანი ხარაჩოების წარმოებისთვის ორი განსხვავებული ფორების ზომით“ მყარი თავისუფალი ფორმის დამზადების (SSF) კომპიუტერული დიზაინის (CAD) გამოყენებით, რათა შეესწავლათ თერაპიული სასახსრე ხრტილის ჩანაცვლება, როგორც „ჩვეულებრივი ქსოვილების აღდგენის ალტერნატივა“. კვლევამ აჩვენა, რომ რაც უფრო მცირეა ფორების ზომა მექანიკურ სტრესთან ერთად ბიორეაქტორში (in vivo-მსგავსი პირობების გამოსაწვევად), მით უფრო მაღალია უჯრედების სიცოცხლისუნარიანობა პოტენციურ თერაპიულ ფუნქციონირებაში აღდგენის დროის შემცირებისა და ტრანსპლანტაციის ეფექტურობის გაზრდის გზით.
ლაზერული დახმარებით ბიობეჭდვა
2012 წელს ჩატარებულ კვლევაში კოხმა და სხვებმა ყურადღება გაამახვილეს იმაზე, შეიძლება თუ არა ლაზერით დამხმარე ბიობეჭდვის (LaBP) გამოყენება ბუნებრივ მატრიცაში მრავალუჯრედიანი 3D ნიმუშების შესაქმნელად და ფუნქციონირებენ თუ არა გენერირებული კონსტრუქტები და ქმნიან თუ არა ქსოვილს. LaBP აწყობს ცოცხალი უჯრედების სუსპენზიების მცირე მოცულობებს მაღალი გარჩევადობის კომპლექტურ ნიმუშებში. კვლევა წარმატებული იყო, მკვლევარები ვარაუდობენ, რომ „გენერირებული ქსოვილოვანი კონსტრუქტები შეიძლება გამოყენებულ იქნას in vivo ტესტირებისთვის ცხოველურ მოდელებში მათი იმპლანტაციით “ (14). ამ კვლევის მონაცემებით, მხოლოდ ადამიანის კანის ქსოვილია სინთეზირებული, თუმცა მკვლევარები ვარაუდობენ, რომ „დაბეჭდილ უჯრედულ კონსტრუქტში სხვა უჯრედების ტიპების (მაგ. , მელანოციტების , შვანის უჯრედების , თმის ფოლიკულის უჯრედების) ინტეგრირებით, შესაძლებელია ამ უჯრედების ქცევის ანალიზი 3D in vitro მიკროგარემოს მსგავს, მათ ბუნებრივ გარემოში“, რაც სასარგებლოა წამლების აღმოჩენისა და ტოქსიკოლოგიური კვლევებისთვის.
თვითაწყობილი რეკომბინანტული ობობას აბრეშუმის ნანომემბრანები
გუსტაფსონმა და სხვებმა აჩვენეს სმ ზომის ფართობის, მაგრამ მხოლოდ 250 ნმ სისქის, დამოუკიდებლად მდგომი, ბიოაქტიური მემბრანები, რომლებიც წარმოიქმნა ობობას აბრეშუმის თვითაწყობით წყალხსნარის საზღვარზე. მემბრანები უნიკალურად აერთიანებს ნანომასშტაბის სისქეს, ბიოდეგრადირებადობას, ულტრამაღალ დაჭიმულობას და სიმტკიცეს, ცილების გამტარიანობას და ხელს უწყობს უჯრედების სწრაფ ადჰეზიას და პროლიფერაციას. მათ აჩვენეს კერატინოციტების თანმიმდევრული ფენის ზრდა. ობობას აბრეშუმის ეს ნანომემბრანები ასევე გამოყენებულია სისხლძარღვის სტატიკური in vitro მოდელის შესაქმნელად.
ქსოვილის ინჟინერია ადგილზე
ქსოვილის ადგილზე რეგენერაცია განისაზღვრება, როგორც ბიომასალების (ცალკე ან უჯრედებთან და/ან ბიომოლეკულებთან კომბინაციაში) იმპლანტაცია ქსოვილის დეფექტში, ორგანიზმის მიმდებარე მიკროგარემოს გამოყენებით, როგორც ბუნებრივი ბიორეაქტორი. ამ მიდგომამ გამოყენება ჰპოვა ძვლის რეგენერაციაში, რაც საშუალებას იძლევა უჯრედული კონსტრუქციების ფორმირების უშუალოდ საოპერაციო ოთახში.
აწყობის მეთოდები
ქსოვილების ინჟინერიაში მუდმივი პრობლემა მასის ტრანსპორტირების შეზღუდვებია. ინჟინერიულ ქსოვილებს, როგორც წესი, არ აქვთ საწყისი სისხლის მიწოდება, რაც ართულებს იმპლანტირებული უჯრედებისთვის საკმარისი ჟანგბადისა და საკვები ნივთიერებების მიღებას გადარჩენის ან სათანადო ფუნქციონირებისთვის.
თვითაწყობა
თვითაწყობის მეთოდები ქსოვილების ინჟინერიისთვის პერსპექტიულ მეთოდებად იქნა მიჩნეული. თვითაწყობის მეთოდებს აქვთ უპირატესობა, რომ ქსოვილებს საშუალებას აძლევს განავითარონ საკუთარი უჯრედგარე მატრიცა, რაც იწვევს ქსოვილის უკეთესად რეპლიკაციას მშობლიური ქსოვილის ბიოქიმიურ და ბიომექანიკურ თვისებებზე. თვითაწყობის ინჟინერიული სასახსრე ხრტილი ჯერი ჰუმ და კირიაკოს ა. ათანასიუმ 2006 წელს შემოიღეს და ამ პროცესის გამოყენებამ გამოიწვია ინჟინერიული ხრტილის შექმნა, რომელიც მშობლიური ქსოვილის სიმტკიცეს უახლოვდება. თვითაწყობა არის ლაბორატორიაში უჯრედების სამგანზომილებიან ფორმებად ასაწყობად მთავარი ტექნოლოგია. ქსოვილების უჯრედებად დასაშლელად, მკვლევარებმა ჯერ უნდა გახსნან უჯრედგარე მატრიცა, რომელიც ჩვეულებრივ მათ ერთმანეთთან აკავშირებს. უჯრედების იზოლირების შემდეგ, მათ უნდა შექმნან რთული სტრუქტურები, რომლებიც ჩვენს ბუნებრივ ქსოვილებს ქმნიან.
თხევადზე დაფუძნებული შაბლონის აწყობა
ფარადეის ტალღებით შექმნილი ჰაერ-თხევადი ზედაპირი შესწავლილია, როგორც შაბლონი ბიოლოგიური ერთეულების ასაწყობად ქვემოდან ზემოთ ქსოვილოვანი ინჟინერიისთვის. ამ სითხეზე დაფუძნებული შაბლონის დინამიურად ხელახლა კონფიგურაცია შესაძლებელია რამდენიმე წამში და შაბლონზე აწყობა შეიძლება განხორციელდეს მასშტაბირებადი და პარალელური გზით. მიკრომასშტაბიანი ჰიდროგელების, უჯრედების, ნეირონებში დათესილი მიკრომატარებლის მძივების, უჯრედული სფეროიდების აწყობა სხვადასხვა სიმეტრიულ და პერიოდულ სტრუქტურებში დემონსტრირებული იყო უჯრედების კარგი სიცოცხლისუნარიანობით. 3-D ნეირონული ქსელის ფორმირება მიღწეული იქნა 14-დღიანი ქსოვილოვანი კულტურის შემდეგ.
დანამატური წარმოება
ბიოლოგიური სისტემების სამგანზომილებიანი და მაღალი სიზუსტის მოდელების სფეროში პიონერები მრავალი პროექტითა და ტექნოლოგიით არიან დანერგილნი, მათ შორის ქსოვილებისა და მთელი ორგანოების შექმნის სწრაფი მეთოდით, რომელიც მოიცავს 3-D პრინტერს, რომელსაც შეუძლია ხარაჩოებისა და უჯრედების ფენა-ფენა ბიობეჭდვა სამუშაო ქსოვილის ნიმუშში ან ორგანოში. მოწყობილობა წარმოდგენილია TED-ზე გამოსვლისას დოქტორი ენტონი ატალას, მედიცინის დოქტორის, უეიკ ფორესტის რეგენერაციული მედიცინის ინსტიტუტის დირექტორის და უეიკ ფორესტის უნივერსიტეტის უროლოგიის დეპარტამენტის ხელმძღვანელის, WH Boyce-ის პროფესორის, მიერ , რომლის დროსაც თირკმელი იბეჭდება სცენაზე სემინარის დროს და შემდეგ წარდგენილია აუდიტორიისთვის. მოსალოდნელია, რომ ეს ტექნოლოგია მომავალში შესაძლებელს გახდის ღვიძლის წარმოებას ტრანსპლანტაციისთვის და თეორიულად ტოქსიკოლოგიისა და სხვა ბიოლოგიური კვლევებისთვისაც.
2015 წელს ხელოვნური ხრტილოვანი კონსტრუქციების ინჟინერიით ინ ვივო ექსპერიმენტებისთვის გამოყენებული იქნა მრავალფოტონიანი დამუშავება (MPP). ექს ვივო ჰისტოლოგიურმა გამოკვლევამ აჩვენა, რომ გარკვეული ფორების გეომეტრია და ქონდროციტების (Cho) წინასწარი ზრდა იმპლანტაციამდე მნიშვნელოვნად აუმჯობესებს შექმნილი სამგანზომილებიანი ხარაჩოების მუშაობას. მიღწეული ბიოშეთავსებადობა შედარებადი იყო კომერციულად ხელმისაწვდომ კოლაგენის მემბრანებთან. ამ კვლევის წარმატებული შედეგი ადასტურებს იმ აზრს, რომ ექვსკუთხა ფორების ფორმის ჰიბრიდული ორგანულ-არაორგანული მიკროსტრუქტურირებული ხარაჩოები ჩოს დათესვასთან ერთად შეიძლება წარმატებით იქნას გამოყენებული ხრტილოვანი ქსოვილის ინჟინერიისთვის.
ბოლო დროს ქსოვილების ინჟინერია ვასკულარიზაციაზე ფოკუსირებით განვითარდა. ორფოტონიან პოლიმერიზაციაზე დაფუძნებული დანამატური წარმოების გამოყენებით, მილისებრი ჰიდროგელის სტრუქტურებიდან იქმნება სინთეზური 3D მიკროსისხლძარღვების ქსელები. ამ ქსელებს შეუძლიათ ქსოვილების რამდენიმე კუბური მილიმეტრის ზომის პერფუზია, რაც უზრუნველყოფს ხანგრძლივ სიცოცხლისუნარიანობას და უჯრედების ზრდას in vitro. ეს ინოვაცია ქსოვილების ინჟინერიაში მნიშვნელოვან წინგადადგმულ ნაბიჯს წარმოადგენს, რაც ხელს უწყობს ადამიანის ქსოვილების რთული მოდელების შემუშავებას.
ხარაჩოები
2013 წელს, სხვადასხვა კონფიგურაციაში Matrigel- ის სამგანზომილებიანი სკაფოლდინგის გამოყენებით , in vitro წარმოიქმნა პანკრეასის მნიშვნელოვანი ორგანოიდები . მცირე რაოდენობის უჯრედების კლასტერები ერთ კვირაში 40 000 უჯრედად გამრავლდა. კლასტერები გარდაიქმნება უჯრედებად, რომლებიც გამოიმუშავებენ საჭმლის მომნელებელ ფერმენტებს ან ჰორმონებს , როგორიცაა ინსულინი , და თვითორგანიზდებიან პანკრეასის მსგავსი განშტოებული პანკრეასის ორგანოიდებად.
უჯრედები მგრძნობიარეა გარემოს მიმართ, როგორიცაა გელის სიმკვრივე და სხვა უჯრედებთან კონტაქტი. ცალკეული უჯრედები არ ხარობენ; ორგანოიდის შემდგომი განვითარებისთვის საჭირო იყო მინიმუმ ოთხი მიმდებარე უჯრედი. გარემოს შემადგენლობის მოდიფიკაციებმა წარმოქმნა ან ღრუ სფეროები, რომლებიც ძირითადად პანკრეასის წინამორბედებისგან შედგება, ან რთული ორგანოიდები, რომლებიც სპონტანურად განიცდიან პანკრეასის მორფოგენეზს და დიფერენციაციას. პანკრეასის წინამორბედების შენარჩუნება და გაფართოება მოითხოვს აქტიურ Notch და FGF სიგნალიზაციას, რაც იმეორებს in vivo ნიშური სიგნალიზაციის ურთიერთქმედებებს.
ორგანოიდები პოტენციურად მინი-ორგანოებად ითვლებოდა ნარკოტიკების ტესტირებისთვის და ინსულინის წარმომქმნელი უჯრედებისთვის.
Matrigel-ის 3-D ხარაჩოების გარდა, შემუშავდა სხვა კოლაგენის გელის სისტემებიც. კოლაგენის/ჰიალურონის მჟავას ხარაჩოები გამოიყენება სარძევე ჯირკვლის მოდელირებისთვის ინ ვიტრო პირობებში, ეპითელური და ადიპოციტების უჯრედების თანაკულტივირებისას. HyStem ნაკრები კიდევ ერთი 3-D პლატფორმაა, რომელიც შეიცავს ექსტრაუჯრედოვანი მატრიქსის კომპონენტებს და ჰიალურონის მჟავას და გამოიყენება კიბოს კვლევისთვის. გარდა ამისა, ჰიდროგელის შემადგენელი ნაწილების ქიმიური მოდიფიცირება შესაძლებელია ჯვარედინი შეკავშირებისა და მათი მექანიკური თვისებების გასაუმჯობესებლად.
ქსოვილის კულტურა
ბევრ შემთხვევაში, ფუნქციური ქსოვილებისა და ბიოლოგიური სტრუქტურების შექმნა in vitro მოითხოვს ფართომასშტაბიან კულტივაციას გადარჩენის, ზრდისა და ფუნქციონალურობის სტიმულირების ხელშესაწყობად. ზოგადად, უჯრედების ძირითადი მოთხოვნილებები უნდა შენარჩუნდეს კულტურაში, რაც მოიცავს ჟანგბადის , pH-ის , ტენიანობის , ტემპერატურის , საკვები ნივთიერებების და ოსმოსური წნევის შენარჩუნებას.
ქსოვილის ინჟინერიით მიღებული კულტურები ასევე დამატებით პრობლემებს წარმოადგენს კულტურული პირობების შენარჩუნების თვალსაზრისით. სტანდარტულ უჯრედულ კულტურაში დიფუზია ხშირად საკვები ნივთიერებებისა და მეტაბოლიტების ტრანსპორტირების ერთადერთი საშუალებაა. თუმცა, როდესაც კულტურა უფრო დიდი და რთული ხდება, როგორც ეს ინჟინერიით მიღებული ორგანოებისა და მთლიანი ქსოვილების შემთხვევაში ხდება, კულტურის შესანარჩუნებლად სხვა მექანიზმებიც უნდა იქნას გამოყენებული, როგორიცაა ქსოვილში კაპილარული ქსელების შექმნა.

ქსოვილის კულტურის კიდევ ერთი პრობლემა ფუნქციონირების ინდუცირებისთვის საჭირო შესაბამისი ფაქტორების ან სტიმულების დანერგვაა. ბევრ შემთხვევაში, მარტივი შემანარჩუნებელი კულტურა საკმარისი არ არის. ზოგჯერ საჭიროა ზრდის ფაქტორები , ჰორმონები , სპეციფიკური მეტაბოლიტები ან საკვები ნივთიერებები, ქიმიური და ფიზიკური სტიმულები. მაგალითად, გარკვეული უჯრედები რეაგირებენ ჟანგბადის დაძაბულობის ცვლილებებზე მათი ნორმალური განვითარების ნაწილად, როგორიცაა ქონდროციტები , რომლებიც უნდა ადაპტირდნენ დაბალი ჟანგბადის პირობებთან ან ჰიპოქსიასთან ჩონჩხის განვითარების დროს. სხვები, როგორიცაა ენდოთელური უჯრედები, რეაგირებენ სითხის ნაკადიდან გამოწვეულ ძვრის სტრესზე , რომელიც გვხვდება სისხლძარღვებში . მექანიკური სტიმულები, როგორიცაა წნევის იმპულსები, სასარგებლოა ყველა სახის გულ-სისხლძარღვთა ქსოვილისთვის, როგორიცაა გულის სარქველები, სისხლძარღვები ან პერიკარდიუმი.
ბიორეაქტორები
უჯრედების პროლიფერაციასა და დიფერენციაციაზე დიდწილად გავლენას ახდენს მიმდებარე უჯრედგარე მატრიქსის გარემოში არსებული მექანიკური და ბიოქიმიური სიგნალები . ბიორეაქტორები, როგორც წესი, შემუშავებულია მზარდი ქსოვილის სპეციფიკური ფიზიოლოგიური გარემოს რეპლიკაციისთვის (მაგ., გულის ქსოვილის ზრდისთვის მოქნილობა და სითხის გადახრა). ამან შეიძლება სპეციალიზებული უჯრედული ხაზების აყვავების საშუალება მისცეს კულტურებში, რომლებიც იმეორებენ მათ მშობლიურ გარემოს, მაგრამ ასევე ბიორეაქტორებს მიმზიდველ ინსტრუმენტებად აქცევს ღეროვანი უჯრედების კულტივირებისთვის . წარმატებული ღეროვან უჯრედებზე დაფუძნებული ბიორეაქტორი ეფექტურია ერთგვაროვანი თვისებების მქონე ღეროვანი უჯრედების გაფართოებისთვის და/ან კონტროლირებადი, რეპროდუცირებადი დიფერენციაციის ხელშეწყობისთვის შერჩეულ მომწიფებულ უჯრედების ტიპებად.
არსებობს ბიორეაქტორების მრავალფეროვნება, რომლებიც შექმნილია 3D უჯრედული კულტურებისთვის. არსებობს პატარა პლასტმასის ცილინდრული კამერები, ასევე მინის კამერები, რეგულირებადი შიდა ტენიანობით და ტენით, რომლებიც სპეციალურად შექმნილია უჯრედების სამ განზომილებაში გასაზრდელად. ბიორეაქტორი იყენებს ბიოაქტიურ სინთეზურ მასალებს, როგორიცაა პოლიეთილენ ტერეფტალატის მემბრანები, რათა შემოახვიოს სფეროიდულ უჯრედებს გარემოში, რომელიც ინარჩუნებს საკვები ნივთიერებების მაღალ დონეს. ისინი ადვილად იხსნება და იხურება, რათა უჯრედის სფეროიდები ამოღებულ იქნას ტესტირებისთვის, თუმცა კამერას შეუძლია შეინარჩუნოს 100%-იანი ტენიანობა მთელ სივრცეში. ეს ტენიანობა მნიშვნელოვანია უჯრედების მაქსიმალური ზრდისა და ფუნქციონირების მისაღწევად. ბიორეაქტორის კამერა უფრო დიდი მოწყობილობის ნაწილია, რომელიც ბრუნავს, რათა უზრუნველყოს უჯრედების თანაბარი ზრდა სამი განზომილების განმავლობაში თითოეული მიმართულებით.
სინგაპურული კომპანია Quintech Life Sciences-ის ფარგლებში, QuinXell Technologies-მა შეიმუშავა ბიორეაქტორი, რომელიც ცნობილია როგორც TisXell Biaxial Bioreactor , რომელიც სპეციალურად ქსოვილების ინჟინერიისთვისაა შექმნილი. ეს არის მსოფლიოში პირველი ბიორეაქტორი, რომელსაც აქვს სფერული მინის კამერა ორღერძიანი ბრუნვით; სპეციალურად საშვილოსნოში ნაყოფის ბრუნვის იმიტაციისთვის; რაც ხელსაყრელ გარემოს ქმნის ქსოვილების ზრდისთვის.
მექანიკური სტიმულაციის მრავალი ფორმა ასევე გაერთიანდა ერთ ბიორეაქტორში. გენის ექსპრესიის ანალიზის გამოყენებით, ერთმა აკადემიურმა კვლევამ აჩვენა, რომ ციკლური დაძაბვისა და ულტრაბგერითი სტიმულაციის კომბინაციის გამოყენება ბიორეაქტორში პრეოსტეობლასტურ უჯრედებზე აჩქარებს მატრიქსის მომწიფებას და დიფერენციაციას. ამ კომბინირებული სტიმულაციის ბიორეაქტორის ტექნოლოგია შეიძლება გამოყენებულ იქნას ძვლის უჯრედების უფრო სწრაფად და ეფექტურად გასაზრდელად მომავალში კლინიკურ ღეროვანი უჯრედების თერაპიებში.
MC2 Biotek-მა ასევე შეიმუშავა ბიორეაქტორი, რომელიც ცნობილია როგორც ProtoTissue , რომელიც იყენებს გაზის გაცვლას უჯრედის კამერაში ჟანგბადის მაღალი დონის შესანარჩუნებლად; ეს აუმჯობესებდა წინა ბიორეაქტორებს, რადგან ჟანგბადის მაღალი დონე ხელს უწყობს უჯრედის ზრდას და ნორმალურ უჯრედულ სუნთქვას .
ბიორეაქტორებზე კვლევის აქტიური სფეროები მოიცავს წარმოების მასშტაბის გაზრდას და ფიზიოლოგიური გარემოს დახვეწას, რაც ორივეს შეუძლია გააუმჯობესოს ბიორეაქტორების ეფექტურობა და ეფექტიანობა კვლევაში ან კლინიკურ გამოყენებაში. ამჟამად ბიორეაქტორები გამოიყენება, სხვა საკითხებთან ერთად, უჯრედული და ქსოვილოვანი დონის თერაპიის, უჯრედებისა და ქსოვილების რეაქციის სპეციფიკურ ფიზიოლოგიურ გარემოში ცვლილებებზე და დაავადებებისა და დაზიანებების განვითარების შესასწავლად.
გრძელი ბოჭკოების წარმოქმნა
2013 წელს, ტოკიოს უნივერსიტეტის ჯგუფმა შეიმუშავა უჯრედებით დატვირთული ბოჭკოები, რომელთა სიგრძე ერთ მეტრამდეა და ზომა დაახლოებით 100 μm . ეს ბოჭკოები შეიქმნა მიკროფლუიდური მოწყობილობის გამოყენებით , რომელიც ქმნის ორმაგ კოაქსიალურ ლამინარურ ნაკადს. მიკროფლუიდური მოწყობილობის თითოეული „შრე“ (უჯრედები დათესილია ექსტრაუჯრედოვან მატრიქსში , ჰიდროგელის გარსში და ბოლოს კალციუმის ქლორიდის ხსნარში). დათესილი უჯრედები კულტივირებულია ჰიდროგელის გარსში რამდენიმე დღის განმავლობაში, შემდეგ გარსი ამოღებულია სიცოცხლისუნარიანი უჯრედული ბოჭკოებით. ექსტრაუჯრედოვანი მატრიქსის ბირთვში შეიყვანეს სხვადასხვა ტიპის უჯრედები, მათ შორის მიოციტები , ენდოთელური უჯრედები , ნერვული უჯრედების ბოჭკოები და ეპითელური უჯრედების ბოჭკოები. ამ ჯგუფმა შემდეგ აჩვენა, რომ ამ ბოჭკოების ერთად ქსოვა შესაძლებელია ქსოვილების ან ორგანოების დასამზადებლად ტექსტილის ქსოვის მსგავსი მექანიზმით . ბოჭკოვანი მორფოლოგია უპირატესობას ანიჭებს იმით, რომ ისინი ტრადიციული ხარაჩოს დიზაინის ალტერნატივას წარმოადგენენ და ბევრი ორგანო (მაგალითად, კუნთი) შედგება ბოჭკოვანი უჯრედებისგან.
ბიოხელოვნური ორგანოები
ფილტვი
ექსტრაკორპორალური მემბრანული ოქსიგენაციის (ECMO) აპარატები, რომლებიც ასევე ცნობილია როგორც გულისა და ფილტვების აპარატები, წარმოადგენს კარდიოფილტვის შუნტირების ტექნიკის ადაპტაციას , რომელიც უზრუნველყოფს გულისა და ფილტვების მხარდაჭერას. ის ძირითადად გამოიყენება ფილტვების ხანგრძლივი, მაგრამ მაინც დროებითი ვადით (1–30 დღე) მხარდასაჭერად და შექცევადი დაავადებებისგან გამოჯანმრთელების უზრუნველსაყოფად. რობერტ ბარტლეტი ცნობილია, როგორც ECMO-ს მამა და მან ახალშობილის პირველი მკურნალობა ECMO აპარატის გამოყენებით 1975 წელს ჩაატარა.
კანი
ქსოვილოვანი ინჟინერიით შექმნილი კანი ბიოხელოვნური ორგანოს სახეობაა, რომელიც ხშირად გამოიყენება დამწვრობის, დიაბეტური ტერფის წყლულების ან სხვა დიდი ჭრილობების სამკურნალოდ, რომლებიც თავისით კარგად ვერ შეხორცდება. ხელოვნური კანის დამზადება შესაძლებელია აუტოტრანსპლანტანტებისგან, ალოტრანსპლანტანტებისგან და ქსენოტრანსპლანტანტებისგან. აუტოტრანსპლანტირებული კანი პაციენტის საკუთარი კანიდან მოდის, რაც დერმას საშუალებას აძლევს უფრო სწრაფად შეხორცდეს, ხოლო დონორის ადგილიდან რამდენჯერმე ხელახლა აღება შესაძლებელია. ალოტრანსპლანტირებული კანი ხშირად გვამური კანიდან მოდის და ძირითადად დამწვრობის მსხვერპლთა სამკურნალოდ გამოიყენება. და ბოლოს, ქსენოტრანსპლანტირებული კანი ცხოველებისგან მოდის და კანის დროებით შეხორცების სტრუქტურას უზრუნველყოფს. ისინი ხელს უწყობენ კანის რეგენერაციას, მაგრამ ვერ გახდებიან მასპინძელი კანის ნაწილი. ქსოვილოვანი ინჟინერიით შექმნილი კანი ამჟამად კომერციული პროდუქტების სახით არის ხელმისაწვდომი. ინტეგრა, რომელიც თავდაპირველად მხოლოდ დამწვრობის სამკურნალოდ გამოიყენებოდა, შედგება კოლაგენის მატრიცისა და ქონდროიტინი სულფატისგან, რომლის გამოყენებაც შესაძლებელია კანის შემცვლელად. ქონდროიტინი სულფატი პროტეოგლიკანების კომპონენტის ფუნქციას ასრულებს, რაც ხელს უწყობს უჯრედგარე მატრიქსის ფორმირებას. ინტეგრას ხელახლა პოპულაცია და რევასკულარიზაცია შესაძლებელია კანის კოლაგენის არქიტექტურის შენარჩუნებით, რაც მას ბიოხელოვნურ ორგანოდ აქცევს. დერმაგრაფტი, კიდევ ერთი კომერციულად წარმოებული ქსოვილოვანი ინჟინერიით შექმნილი კანის პროდუქტი, დამზადებულია ცოცხალი ფიბრობლასტებისგან. ეს ფიბრობლასტები მრავლდებიან და გამოიმუშავებენ ზრდის ფაქტორებს, კოლაგენს და ECM ცილებს, რომლებიც ხელს უწყობენ გრანულაციური ქსოვილის აგებას.
გული
ვინაიდან გულის გადანერგვის მომლოდინე პაციენტების რაოდენობა დროთა განმავლობაში მუდმივად იზრდება და მომლოდინე სიაში მყოფი პაციენტების რაოდენობა აღემატება ორგანოების ხელმისაწვდომობას, ხელოვნური ორგანოები, რომლებიც გამოიყენება როგორც ჩანაცვლებითი თერაპია ტერმინალური გულის უკმარისობის დროს, ხელს შეუწყობს ამ სირთულის შემსუბუქებას. ხელოვნური გულები ჩვეულებრივ გამოიყენება გულის გადანერგვის შემდეგ ან შეიძლება გამოყენებულ იქნას როგორც ჩანაცვლებითი თერაპია ტერმინალური გულის უკმარისობის დროს. ხელოვნური გული (TAH), რომელიც პირველად დოქტორმა ვლადიმერ პ. დემიხოვმა 1937 წელს შემოიღო, იდეალურ ალტერნატივად იქცა. მას შემდეგ ის შემუშავდა და გაუმჯობესდა, როგორც მექანიკური ტუმბო, რომელიც უზრუნველყოფს ხანგრძლივ სისხლის მიმოქცევის მხარდაჭერას და ცვლის დაავადებულ ან დაზიანებულ გულის პარკუჭებს, რომლებსაც არ შეუძლიათ სისხლის სწორად გადატუმბვა, რითაც აღადგენს ფილტვის და სისტემურ ნაკადს. ზოგიერთ ამჟამინდელ TAH-ს მოიცავს AbioCor-ს, FDA-ს მიერ დამტკიცებულ მოწყობილობას, რომელიც შედგება ორი ხელოვნური პარკუჭისა და მათი სარქველებისგან და არ საჭიროებს კანქვეშა კავშირებს და ნაჩვენებია ორპარკუჭიანი გულის უკმარისობის მქონე პაციენტებისთვის. 2010 წელს SynCardia-მ გამოუშვა პორტატული თავისუფლების დრაივერი, რომელიც პაციენტებს საშუალებას აძლევს, ჰქონდეთ პორტატული მოწყობილობა საავადმყოფოში გამოკეტვის გარეშე.
თირკმელი
მიუხედავად იმისა, რომ თირკმლის გადანერგვა შესაძლებელია, თირკმლის უკმარისობის მკურნალობა უფრო ხშირად ხელოვნური თირკმლის გამოყენებით ხდება. პირველი ხელოვნური თირკმელები და ამჟამად გამოყენებული თირკმელების უმეტესობა ექსტრაკორპორალურია, მაგალითად, ჰემოდიალიზის, რომელიც სისხლს პირდაპირ ფილტრავს, ან პერიტონეალური დიალიზის, რომელიც მუცლის ღრუში არსებული სითხის მეშვეობით ფილტრავს. თირკმლის ბიოლოგიურ ფუნქციებში, როგორიცაა მეტაბოლური ფაქტორების ან ჰორმონების გამომუშავება, წვლილის შესატანად, ზოგიერთი ხელოვნური თირკმელი თირკმლის უჯრედებს იყენებს. პროგრესი შეინიშნება ამ მოწყობილობების უფრო პატარა და ტრანსპორტირებადი, ან თუნდაც იმპლანტირებადი გახდომის კუთხით . ერთ-ერთი გამოწვევა, რომელიც ჯერ კიდევ უნდა გადაიჭრას ამ მცირე ზომის მოწყობილობებთან დაკავშირებით, არის შეზღუდული მოცულობის და შესაბამისად, შეზღუდული ფილტრაციის შესაძლებლობების წინააღმდეგ ბრძოლა.
ასევე დანერგილია ბიოსკაფოლდები, რათა შეიქმნას ჩარჩო, რომლის საფუძველზეც შესაძლებელია ნორმალური თირკმლის ქსოვილის რეგენერაცია. ეს სკაფოლდები მოიცავს ბუნებრივ სკაფოლდებს (მაგ., დეცელულალიზებულ თირკმელებს, კოლაგენის ჰიდროგელს, ან აბრეშუმის ფიბროინს ), სინთეზურ სკაფოლდებს (მაგ., პოლი[რძემჟავა-კო-გლიკოლის მჟავა] ან სხვა პოლიმერებს) ან ორი ან მეტი ბუნებრივი და სინთეზური სკაფოლდის კომბინაციას. ამ სკაფოლდების იმპლანტაცია ორგანიზმში შესაძლებელია უჯრედების დამუშავების გარეშე ან ღეროვანი უჯრედების დათესვისა და ინკუბაციის პერიოდის შემდეგ. ტარდება ინ ვიტრო და ინ ვივო კვლევები სკაფოლდის ტიპის შესადარებლად და ოპტიმიზაციისთვის და იმის შესაფასებლად, ზრდის თუ არა იმპლანტაციამდე უჯრედების დათესვა თირკმელების სიცოცხლისუნარიანობას, რეგენერაციას და ეფექტურ ფუნქციას. ბოლოდროინდელმა სისტემატურმა მიმოხილვამ და მეტაანალიზმა შეადარა ცხოველებზე გამოქვეყნებული კვლევების შედეგები და დაადგინა, რომ გაუმჯობესებული შედეგები აღინიშნება ჰიბრიდული (შერეული) სკაფოლდების და უჯრედების დათესვის გამოყენებით; თუმცა, ამ შედეგების მეტაანალიზი არ შეესაბამებოდა მიმოხილვის აღწერითი შედეგების შეფასებას. ამიტომ, მიზანშეწონილია უფრო დიდი ცხოველებისა და ახალი სტრუქტურების მონაწილეობით შემდგომი კვლევების ჩატარება და წინა კვლევების უფრო გამჭვირვალე რეპროდუცირება.
ბიომიმეტიკა
ბიომიმეტიკა არის დარგი, რომლის მიზანია ისეთი მასალებისა და სისტემების წარმოება, რომლებიც იმეორებენ ბუნებაში არსებულ მასალებს. ქსოვილების ინჟინერიის კონტექსტში, ეს არის ინჟინრების მიერ გამოყენებული გავრცელებული მიდგომა ამ აპლიკაციებისთვის მასალების შესაქმნელად, რომლებიც შედარებადია მშობლიურ ქსოვილებთან მათი სტრუქტურის, თვისებებისა და ბიოშეთავსებადობის თვალსაზრისით. მასალის თვისებები დიდწილად დამოკიდებულია ამ მასალის ფიზიკურ, სტრუქტურულ და ქიმიურ მახასიათებლებზე. შესაბამისად, სისტემის დიზაინისადმი ბიომიმეტიკური მიდგომა მნიშვნელოვანი გახდება მასალების ინტეგრაციისთვის და საჭირო იქნება ბიოლოგიური პროცესებისა და ურთიერთქმედებების საკმარისი გაგება. ბიოლოგიური სისტემებისა და პროცესების რეპლიკაცია ასევე შეიძლება გამოყენებულ იქნას ბიო-ინსპირირებული მასალების სინთეზში, რათა მივაღწიოთ სასურველ ბიოლოგიურ მასალას. ამიტომ, თუ სინთეზირებულია მასალა, რომელსაც აქვს ბიოლოგიური ქსოვილების იგივე მახასიათებლები, როგორც სტრუქტურულად, ასევე ქიმიურად, მაშინ იდეალურ შემთხვევაში სინთეზირებულ მასალას ექნება მსგავსი თვისებები. ამ ტექნიკას აქვს ვრცელი ისტორია, რომელიც წარმოიშვა ბუნებრივი ფენომენის, როგორც ადამიანის პრობლემების გადაჭრის დიზაინის შთაგონების იდეიდან. ტექნოლოგიის მრავალი თანამედროვე მიღწევა შთაგონებულია ბუნებითა და ბუნებრივი სისტემებით, მათ შორის თვითმფრინავებით, ავტომობილებით, არქიტექტურით და სამრეწველო სისტემებითაც კი. ნანოტექნოლოგიის განვითარებამ ამ ტექნიკის გამოყენება მიკრო და ნანომასშტაბიან პრობლემებში დაიწყო, მათ შორის ქსოვილების ინჟინერიაში. ეს ტექნიკა გამოყენებული იქნა სინთეზური ძვლოვანი ქსოვილების, სისხლძარღვთა ტექნოლოგიების, ხარაჩოების მასალებისა და ინტეგრაციის ტექნიკის, ასევე ფუნქციონალიზებული ნანონაწილაკების შესამუშავებლად.
ნეირონული ქსელების აგება რბილ მასალაში
2018 წელს, ბრანდეისის უნივერსიტეტის მეცნიერებმა გამოაქვეყნეს თავიანთი კვლევა ქიმიური ქსელებით ჩასმული რბილი მასალის შესახებ, რომელსაც შეუძლია ნერვული ქსოვილის გლუვი და კოორდინირებული ქცევის იმიტაცია. ეს კვლევა დაფინანსდა აშშ-ის არმიის კვლევითი ლაბორატორიის მიერ . მკვლევარებმა წარმოადგინეს ნეირონული ქსელების ექსპერიმენტული სისტემა, რომელიც თეორიულად მოდელირებულია, როგორც რეაქცია-დიფუზიის სისტემები . ქსელებში იყო შაბლონური რეაქტორების მასივი, რომელთაგან თითოეული ასრულებდა ბელუსოვ-ჟაბოტინსკის (BZ) რეაქციას. ამ რეაქტორებს შეეძლოთ ნანოლიტრის მასშტაბით ფუნქციონირება.
მკვლევარები აცხადებენ, რომ მათი პროექტის შთაგონება ლურჯი ლენტისებრი გველთევზას მოძრაობა იყო . გველთევზას მოძრაობები კონტროლდება ელექტრული იმპულსებით, რომლებიც განისაზღვრება ნეირონული ქსელების კლასით, რომელსაც ცენტრალური შაბლონების გენერატორი ეწოდება . ცენტრალური შაბლონების გენერატორები ფუნქციონირებენ ვეგეტატიურ ნერვულ სისტემაში , რათა აკონტროლონ სხეულის ისეთი ფუნქციები, როგორიცაა სუნთქვა, მოძრაობა და პერისტალტიკა .
შემუშავებული რეაქტორის თვისებები იყო ქსელის ტოპოლოგია, სასაზღვრო პირობები , საწყისი პირობები, რეაქტორის მოცულობა, შეერთების სიძლიერე და რეაქტორის სინაფსური პოლარობა (მისი ქცევა ინჰიბიტორული თუ აღმგზნებია). შემუშავებული იქნა მყარი ელასტომერის პოლიდიმეთილსილოქსანის (PDMS) BZ ემულსიური სისტემა. როგორც სინათლის, ასევე ბრომის გამტარი PDMS აღწერილია, როგორც ნეირონული ქსელებისთვის პეისმეკერის შესაქმნელად სიცოცხლისუნარიანი მეთოდები.
ბაზარი
ქსოვილების ინჟინერიის ბაზრის ისტორია შეიძლება დაიყოს სამ ძირითად ნაწილად. 2000-იანი წლების დასაწყისში ბიოტექნოლოგიური ბაზრის კრახამდელი პერიოდი, კრახი და შემდგომი პერიოდი.
დასაწყისი
ქსოვილების ინჟინერიის კვლევაში ადრეული პროგრესის უმეტესი ნაწილი აშშ-ში იქნა მიღწეული. ეს განპირობებულია ღეროვანი უჯრედების კვლევასთან დაკავშირებული ნაკლებად მკაცრი რეგულაციებით და სხვა ქვეყნებთან შედარებით უფრო მეტი დაფინანსებით. ეს იწვევს აკადემიური სტარტაპების შექმნას, რომელთაგან ბევრი ჰარვარდიდან ან MIT- დან მოდის . მაგალითად, BioHybrid Technologies-ს, რომლის დამფუძნებელი, ბილ ჩიკი, ჰარვარდის სამედიცინო სკოლაში სწავლობდა და ხელოვნური პანკრეასის შექმნაზე იყო ორიენტირებული. კიდევ ერთი მაგალითია Organogenesis Inc., რომლის დამფუძნებელი MIT-ში სწავლობდა და კანის ინჟინერიის პროდუქტებზე მუშაობდა. MIT-თან კავშირში მყოფი სხვა კომპანიებია TEI Biosciences, Therics და Guilford Pharmaceuticals. 1980-იან წლებში ბიოტექნოლოგიებისადმი განახლებული ინტერესი ბევრ კერძო ინვესტორს ამ ახალ ტექნოლოგიებში ინვესტიციების ჩადებისკენ უბიძგებს, მიუხედავად იმისა, რომ ამ ადრეული სტარტაპების ბიზნეს მოდელები ხშირად არ იყო ძალიან მკაფიო და არ წარმოადგენდა გრძელვადიანი მომგებიანობის გზას. სამთავრობო სპონსორები უფრო თავშეკავებულები იყვნენ დაფინანსებაში, რადგან ქსოვილების ინჟინერია მაღალი რისკის მქონე ინვესტიციად ითვლებოდა.
დიდ ბრიტანეთში ბაზარი უფრო ნელა დაიწყო, მიუხედავად იმისა, რომ ღეროვანი უჯრედების კვლევის რეგულაციებიც მკაცრი არ იყო. ეს ძირითადად იმით არის განპირობებული, რომ ინვესტორების უმეტესობა ნაკლებად იყო მზად ინვესტიციები ჩაედოთ ამ ახალ ტექნოლოგიებში, რომლებიც მაღალი რისკის შემცველ ინვესტიციებად ითვლებოდა. [ 117 ] ბრიტანული კომპანიების წინაშე მდგარი კიდევ ერთი პრობლემა იყო ჯანდაცვის ეროვნული სამსახურისგან მათი პროდუქციის საფასურის გადახდა. ეს განსაკუთრებით იმიტომ ხდება, რომ ჯანდაცვის ეროვნული სამსახური ყველა მხარდაჭერილ პროდუქტზე ხარჯთეფექტურობის ანალიზს ატარებს. ახალი ტექნოლოგიები ხშირად ამ მხრივ კარგად არ მუშაობს.
იაპონიაში მარეგულირებელი სიტუაცია საკმაოდ განსხვავებული იყო. უჯრედების კულტივაცია თავდაპირველად მხოლოდ საავადმყოფოს გარემოში იყო დაშვებული, ხოლო სახელმწიფო უნივერსიტეტებში დასაქმებულ აკადემიურ მეცნიერებს 1998 წლამდე გარე დასაქმების უფლება არ ჰქონდათ. გარდა ამისა, იაპონიის ხელისუფლებას ახალი პრეპარატებისა და მკურნალობის მეთოდების დამტკიცებას უფრო მეტი დრო დასჭირდა, ვიდრე მათ აშშ-სა და ევროპელ კოლეგებს.
ამ მიზეზების გამო, იაპონური ბაზრის ადრეულ ეტაპზე, ყურადღება ძირითადად იაპონიის სხვა ქვეყნებში უკვე დამტკიცებული პროდუქტების მიღებასა და მათ გაყიდვაზე იყო გამახვილებული. აშშ-ის ბაზრისგან განსხვავებით, იაპონიაში ადრეული მოთამაშეები ძირითადად დიდი ფირმები ან ასეთი დიდი ფირმების ქვეკომპანიები იყვნენ, როგორიცაა J-TEC, Menicon და Terumo, და არა მცირე სტარტაპები. 2014 წელს მარეგულირებელი ცვლილებების შემდეგ, რომლებმაც უჯრედების საავადმყოფოს გარეთ კულტივირება დაუშვა, იაპონიაში კვლევის სიჩქარე გაიზარდა და იაპონურმა კომპანიებმაც დაიწყეს საკუთარი პროდუქტების შემუშავება.
ავარია
დიდი ბუმის შემდეგ მალევე, პირველი პრობლემები გამოჩნდა. პრობლემები იყო პროდუქტების FDA-ს მიერ დამტკიცების მიღებასთან დაკავშირებით და თუ ისინი დამტკიცდებოდა, ხშირად სირთულეები იყო სადაზღვევო პროვაიდერების მიერ პროდუქტების საფასურის გადახდისა და ჯანდაცვის პროვაიდერების მიერ მათი მიღების უზრუნველყოფასთან დაკავშირებით.
მაგალითად, ორგანოგენეზს პრობლემები შეექმნა პროდუქტის მარკეტინგსა და ჯანდაცვის სისტემაში ინტეგრირებასთან დაკავშირებით. ეს ნაწილობრივ განპირობებული იყო ცოცხალი უჯრედების დამუშავების სირთულეებით და ექიმებისთვის ამ პროდუქტების ტრადიციულ მეთოდებთან შედარებით გამოყენებისას გაზრდილი სირთულეებით.
კიდევ ერთი მაგალითია Advanced Tissue Sciences-ის Dermagraft-ის კანის პროდუქტი, რომელზეც სადაზღვევო კომპანიების მიერ ანაზღაურების გარეშე საკმარისად მაღალი მოთხოვნა ვერ შეიქმნა. ამის მიზეზები იყო 4000 დოლარის ფასი და ის გარემოება, რომ Advanced Tissue Sciences-ს უჭირდა თავისი პროდუქტის ექიმებისთვის ცნობადობის გაზრდა.
ზემოთ მოყვანილი მაგალითები აჩვენებს, თუ როგორ უჭირდათ კომპანიებს მოგების მიღება. ეს, თავის მხრივ, ინვესტორებს მოთმინების დაკარგვამდე და შემდგომი დაფინანსების შეჩერებამდე აიძულებს. შედეგად, 2000-იანი წლების დასაწყისში ქსოვილების ინჟინერიის რამდენიმე კომპანიამ, როგორიცაა Organogenesis-ი და Advanced Tissue Sciences-ი, გაკოტრება გამოაცხადა. ამ დროს, ესენი იყვნენ ერთადერთები, რომლებსაც ბაზარზე კომერციული კანის მოვლის საშუალებები ჰქონდათ.
ხელახლა გამოჩენა
გაკოტრებული ან გაჭირვებული კომპანიების ტექნოლოგიებს ხშირად სხვა კომპანიები ყიდულობდნენ, რომლებიც განვითარებას უფრო კონსერვატიული ბიზნეს მოდელებით აგრძელებდნენ. კომპანიების მაგალითები, რომლებმაც თავიანთი პროდუქცია გაკოტრების შემდეგ გაყიდეს, იყო Curis და Intercytex.
ბევრმა კომპანიამ მიატოვა სრულად ფუნქციონალური ორგანოების შემუშავების გრძელვადიანი მიზნები და მოკლევადიან პერიოდში მოგების მომტანი პროდუქტებისა და ტექნოლოგიების სასარგებლოდ გადაიფიქრა. ამ ტიპის პროდუქტების მაგალითებია კოსმეტიკური და ტესტირების ინდუსტრიის პროდუქტები.
სხვა შემთხვევებში, მაგალითად, Advanced Tissue Sciences-ის შემთხვევაში, დამფუძნებლებმა ახალი კომპანიები დააარსეს.
2010-იან წლებში მარეგულირებელმა ჩარჩომ ასევე დაიწყო ბაზარზე გასვლის დაჩქარების ხელშეწყობა, განსაკუთრებით აშშ-ში, რადგან FDA-მ შექმნა ახალი ცენტრები და გზები, რომლებიც სპეციალურად ცოცხალი უჯრედებიდან მიღებული პროდუქტებისთვის იყო განკუთვნილი, როგორიცაა ბიოლოგიური პროდუქტების შეფასებისა და კვლევის ცენტრი .
ქსოვილების ინჟინერიის პირველი პროდუქტები კომერციულად მომგებიანი გახდა 2010-იან წლებში.
რეგულაცია
ევროპაში რეგულირება ამჟამად სამ სფეროდ იყოფა: სამედიცინო მოწყობილობები , სამკურნალო პროდუქტები და ბიოლოგიური პროდუქტები . ქსოვილოვანი ინჟინერიის პროდუქტები ხშირად ჰიბრიდული ხასიათისაა, რადგან ისინი ხშირად უჯრედებისა და საყრდენი სტრუქტურისგან შედგება. მიუხედავად იმისა, რომ ზოგიერთი პროდუქტის დამტკიცება შესაძლებელია, როგორც სამკურნალო პროდუქტის, სხვები კი სამედიცინო მოწყობილობების დამტკიცებას საჭიროებენ. დერკსენი თავის ნაშრომში განმარტავს, რომ ქსოვილოვანი ინჟინერიის მკვლევარები ზოგჯერ ისეთ რეგულაციებს აწყდებიან, რომლებიც ქსოვილოვანი ინჟინერიის მახასიათებლებს არ შეესაბამება.
ევროპაში შეინიშნება ახალი მარეგულირებელი რეჟიმები, რომლებიც ამ საკითხებს წყვეტენ. ამ საკითხში მარეგულირებელი კონსენსუსის მიღწევის სირთულეების ახსნას იძლევა დიდ ბრიტანეთში ჩატარებული კვლევა. ავტორები ამ პრობლემებს სხვა ტექნოლოგიებთან, როგორიცაა ქსენოტრანსპლანტაცია, მჭიდრო კავშირსა და გადაფარვას მიაწერენ . ამიტომ, მარეგულირებელი ორგანოები მას ცალკე ვერ განიხილავენ. რეგულირებას კიდევ უფრო ართულებს ამ და მასთან დაკავშირებული კვლევის სფეროებთან დაკავშირებული ეთიკური დავები (მაგ., ღეროვანი უჯრედების დავა , ორგანოების ტრანსპლანტაციის ეთიკა ). ზემოთ აღნიშნული კვლევა აუტოლოგიური ხრტილის ტრანსპლანტაციის მაგალითზე აჩვენებს, რომ კონკრეტული ტექნოლოგია შეიძლება ჩაითვალოს „სუფთად“ ან „დაბინძურებულად“ იმავე სოციალური აქტორის მიერ.
ევროკავშირში ქსოვილების ინჟინერიასთან დაკავშირებით ყველაზე აქტუალურია ორი მარეგულირებელი მოძრაობა . ესენია ადამიანის ქსოვილების მოპოვებისა და დამუშავების ხარისხისა და უსაფრთხოების სტანდარტების შესახებ დირექტივა 2004/23/EC , რომელიც ევროპარლამენტმა 2004 წელს მიიღო და ადამიანის ქსოვილების ინჟინერიით მიღებული პროდუქტების შესახებ შემოთავაზებული რეგულაცია. ეს უკანასკნელი შემუშავდა ევროკომისიის საწარმოო დირექტორატის ეგიდით და წარმოდგენილი იქნა ბრიუსელში 2004 წელს.







Комментариев нет:
Отправить комментарий