ცოდნა სინათლეა - Knowledge is light - Знание свет -
| ზოგადი თვისებები | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| მარტივი ნივთიერების ვიზუალური აღწერა | თეთრი მბზინვარე რბილი ლითონი | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| სტანდ. ატომური წონა Ar°(Cd) | 112.414±0.004 112.41±0.01 (დამრგვალებული) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| კადმიუმი პერიოდულ სისტემაში | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ატომური ნომერი (Z) | 48 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ჯგუფი | 12 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| პერიოდი | 5 პერიოდი | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ბლოკი | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ელექტრონული კონფიგურაცია | [Kr] 4d10 5s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ელექტრონი გარსზე | 2, 8, 18, 18, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ელემენტის ატომის სქემა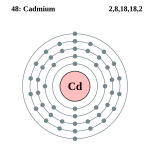 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ფიზიკური თვისებები | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| აგრეგეგატული მდგომ. ნსპ-ში | მყარი სხეული | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| დნობის ტემპერატურა | 321.07 °C (594.22 K, 609.93 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| დუღილის ტემპერატურა | 767 °C (1040 K, 1413 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| სიმკვრივე (ო.ტ.) | 8.65 გ/სმ3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| სიმკვრივე (ლ.წ.) | 7.996 გ/სმ3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| დნობის კუთ. სითბო | 6.21 კჯ/მოლი | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| აორთქ. კუთ. სითბო | 99.87 კჯ/მოლი | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| მოლური თბოტევადობა | 26.020 ჯ/(მოლი·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ნაჯერი ორთქლის წნევა
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ატომის თვისებები | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ჟანგვის ხარისხი | −2, +1, +2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ელექტროდული პოტენციალი | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ელექტროუარყოფითობა | პოლინგის სკალა: 1.69 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| იონიზაციის ენერგია |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ატომის რადიუსი | ემპირიული: 151 პმ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| კოვალენტური რადიუსი (rcov) | 144±9 პმ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ვან-დერ-ვალსის რადიუსი | 158 პმ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
კადმიუმის სპექტრალური ზოლები | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| სხვა თვისებები | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ბუნებაში გვხვდება | პირველადი ნუკლიდების სახით | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| მესრის სტრუქტურა | მჭიდრო ჰექსაგონალური | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ბგერის სიჩქარე | 2310 მ/წმ (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| თერმული გაფართოება | 30.8 µმ/(მ·K) (25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| თბოგამტარობა | 96.6 ვტ/(მ·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| კუთრი წინაღობა | 72.7 ნომ·მ (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| მაგნეტიზმი | დიამაგნეტიკი | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| მაგნიტური ამთვისებლობა | −19.8×10−6 სმ3/მოლ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| იუნგას მოდული | 50 გპა | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| წანაცვლების მოდული | 19 გპა | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| დრეკადობის მოდული | 42 გპა | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| პუასონის კოეფიციენტი | 0.30 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| მოოსის მეთოდი | 2.0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ბრინელის მეთოდი | 203–220 მპა | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS ნომერი | 7440-43-9 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ისტორია | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| აღმომჩენი და პირველი მიმღებია | კარლ სამუელ ჰერმანი და ფრიდრიხ შტრომაიერი (1817) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| სახელი დაარქვა | ფრიდრიხ შტრომაიერი (1817) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| კადმიუმის მთავარი იზოტოპები | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
კადმიუმი (ლათ. Cadmium; ქიმიური სიმბოლო — ) — ელემენტთა პერიოდული სისტემის მეხუთე პერიოდის, მეთორმეტე ჯგუფის (მოძველებული კლასიფიკაციით — მეორე ჯგუფის თანაური ქვეჯგუფის, IIბ) ქიმიური ელემენტი. მისი ატომური ნომერია 48, ატომური მასა — 112.41, tდნ — 321.07 °C, tდუღ — 767 °C, სიმკვრივე — 8.65 გ/სმ3. თეთრი მბზინვარე რბილი ლითონი. ბუნებრივი კადმიუმი შედგება ექვსი სტაბილური (, , , , და ) და ორი სუსტად რადიოაქტიული და იზოტოპისაგან. მშრალ ჰაერზე მდგრადია, ტენიან ჰაერზე მასზე ჩნდება კადმიუმის ოქსიდის თხელი ფენა, რომელიც ხელს უშლის მის შემდგომ ჟანგვას. 1817 წელს აღმოაჩინეს გერმანელმა ქიმიკოსებმა ფ. შტრომაიერმა და 1818 წელს მისგან დამოუკიდებლად კ. ჰერმანმა, კ კარსტენმა და ვ. მაისნერმა.
აღმოჩენის ისტორია
აღმოჩენილია გერმანელი პროფესორის ფრიდრიხ შტომეიერის მიერ 1817 წ. მაგდებურგის პროვიზორებმა თუთიის ოქსიდის ZnO შესწავლისას იეჭვიანეს მასში დარიშხანის მინარევის არსებობა. შტრომეიერმა გამოჰყო ZnO-საგან მუქი-ყავისფერი ოქსიდი, წყალბადით აღადგინა ის და მიიღო მოვერცხლისფრო-თეთრი ფერის ლითონი, რომელმაც მიიღო სახელწოდება - კადმიუმი.
სახელწოდების წარმომავლობა
შტრომაიერმა კადმიუმი დაარქვა მადნის ბერძნული სახელწოდების მიხედვით, საიდანაც გერმანიაში მოიპოვებდნენ თუთიას, — καδμεία. თავის მხრივ, მადანმა სახელწოდება მიიღო კადმის ძველბერძნული მითოლოგიის გმირის პატივსაცემად.
ბუნებაში
კადმიუმის საშუალო შემცველობა დედამიწის ქერქში შეადგენს 130 მგრ/ტ, ზღვის წყალში 0,11 მკგ/ლ. კადმიუმი მიეკუთვნება იშვიათ, გაბნეულ ელემენტებს: მას ბევრი მინერალი შეიცავს იზომორფული მინარევის სახით და ყოველთვის იმყოფება თუთიის მადნებში. ცნობილია მხოლოდ კადმიუმის 6 მინერალი. კადმიუმის ძალიან იშვიათ მინერალებს წარმოადგენენ გრინოკიტი CdS (77,8% Cd), ჰოულიიტიт, ოტავიტი CdCO3, მონტემპონიტი CdO (87,5% Cd), კადმოსელიტი CdSe (47% Cd), ქსანტოხროიტი CdS(H2O)х (77,2% Cd). კადმიუმის ძირითადი მასა გაბნეულია ბევრ მინერალებში (50-ზე მეტი), უპირატესად თუთიის, ტყვიის, სპილენძის, რკინის, მანგანუმის და ვერცხლისწყლის სულფიდებში. კადმიუმის მაქსიმალური კონცეტრაცია შეინიშნება თუთიის მინერალებში და, უპირველეს ყოვლისა, სფალერიტში (5%-მდე). უმეტეს შემთხვევაში კი კადმიუმის შემცველობა სფალერიტში არ აღემატება 0,4 – 0,6%. სხვა სულფიდებში, მაგალითად, სტანინში კადმიუმი არის მიახლოებით 0,003 – 0,2%, გალენიტში 0,005 – 0,02%, ჰალკოპირიტში 0,006 – 0,12%; ამ სულფიდებიდან კადმიუმს ჩვეულებრივ არ გამოყოფენ.
კადმიუმი არ წარმოქმნის დამოუკიდებელ საბადოებს, და შედის სხვა ლითონების საბადოების შემადგენლობაში. კადმიუმის შემცველობა შედარებით მაღალია საშუალოტემპერატურულ ტყვია-თუთიის საბადოებში და ნაწილობრივ სპილენძ-კოლჩედანის საბადოებში .
მიღება
ერთადერთი მინერალი, რომელიც საინტერესოა კადმიუმის მისაღებად არის - გრინოკიტი, ეგრეთ წოდებული "კადმიუმის მატყუარა». მას მოიპოვებენ სფალერიტთან ერთად თუთიის მადნების გადამუშავებისას. გადამუშავებისას კადმიუმი გროვდება პროცესის თანაურ პროდუქტებში, საიდანაც შემდეგ მას გამოჰყოფენ. ახლა წელიწადში ხდება 10³ ტონაზე მეტი კადმიუმის წარმოება.
ფიზიკური თვისებები
კადმიუმი — მოვერცხლისფრო-თეთრი რბილი ლითონია რომელსაც ჰექსაგონალური კრისტალური მესერი აქვს. თუკი კადმიუმის ჯოხს მოვღუნავთ, მაშინ გავიგებთ გაბზარვის ხმას - ეს ლითონის მიკროკრისტალები ეხახუნებიან ერთმანეთს (ასევე ხმაურობს კალას ჯოხიც).
ქიმიური თვისებები
კადმიუმი პერიოდულ სისტემაში იმავე ჯგუფშია სადაც, თუთია და ვერცხლისწყალი, და უჭირავს შუალედური ადგილი მათ შორის, ამიტომაც ამ ელემენტების ზოგი ქიმიური თვისებები მსგავსია. ამ ელემენტების სულფიდები და ოქსიდები წყალში პრაქტიკულად უხსნადია. კადმიუმი ნახშირბადთან არ ურთიერთქმედებს და არ წარმოქმნის კარბიდებს.
გამოყენება
შენადნობები
კადმიუმი გამოიყენება როგორც მაგარი სარჩილავების კომპონენტი (შენადნობები ვერცხლის, სპილენძის და თუთიის საფუძველზე) მათი დნობის ტემპერათურის დასაწევად. წარმოებული კადმიუმის მიახლოებით 10 % არის — საიუველირო შენადნობის და ადვილადლღვობადი შენადნობების კომპონენტი. კადმიუმისა და ოქროს შენადნობს აქვს მომწვანო ფერი.
დამცავი საფარები
წარმოებული კადმიუმის 40 % გამოიყენება ლითონებზე ანტიკოროზიული საფარის დასატანებლად.
დენის ქიმიური წყაროები
კადმიუმის მიახლოებით 20 % მიდის კადმიუმიანი ელექტროდების დასამზადებლად, რომლებიც გამოიყენება აკუმულატორებში (ნიკელ-კადმიუმის აკუმულატორი და ვერცხლი-კადმიუმის აკუმულატორი), ვესტონის ნორმალურ ელემენტებში, სარეზერვო ბატერეებში (ტყვია-კადმიუმის ელემენტი, ვერცხლისწყალი-კადმიუმის ელემენტი) და სხვა.
პიგმენტები
კადმიუმის მიახლოებით 20 % გამოიყენება არაორგანულ საღებავ ნივთიერებებში (სულფიდები და სელენიდები, არეული მარილები, მაგალითად, კადმიუმის სულფიდი — ლიმონის კადმიუმი).
მედიცინა
- ზოგჯერ კადმიუმი გამოიყენება ექსპერიმენტარულ მედიცინაში.
კადმიუმი გამოიყენება ჰომეოპატიურ მედიცინაში.
- ბოლო წლებში კადმიუმს გამოიყენებენ ახალი სიმსივნის საწინააღმდეგო ნანო-მედიკამენტების წარმოებაში სსრკ-ში 1950—ან წლებში ჩატარებული იქნა პირველი წარმატებული ექსპერიმენტები, რომელიც დაკავშირებული იყო სიმსივნის საწინააღმდეგო მედიკამენტების შემუშავებასთან, კადმიუმის ნაერთების საფუძველზე.
ღირებულება
კადმიუმზე ფასი 2011 წელს შეადგინა მიახლოებით 3$ - 1 კგ.
გამოყენების სხვა სფეროები
- კადმიუმის სულფიდი გამოიყენება აპკურ მზის ბატარეებში რომლის მარგი ქმედების კოეფიციენტია მიახლოებით 10—16 %, ასევე როგორც ძალიან კარგი თერმოელექტრული მასალა.
- კადმიუმი გამოიყენება როგორც ნახევარგამტარი მასალების და ლუმინოფორების კომპონენტი.
- კადმიუმი ძალიან კარგად იტაცებს სითბურ ნეიტრონებს და გამოიყენებენ ატომური რეაქტორების რეგულირებადი ღერძის დასამზადებლად ასევე როგორც ნეიტრონებისაგან დასაცავად. ზოგჯერ ეს თვისებები გამოიყენება სიმსივნის საწინააღმდეგო თერაპიის ექსპერიმენტალურ მოდელებში Neutron Capture Therapy
- კადმიუმის ფტორობორატი — მნიშვნელოვანი ფლუსია, გამოიყენება ალუმინისა და სხვა ლითონების რჩილვის დროს.
- კადმიუმის თბოგამტარობა აბსოლუტურ ნულთან ყველა ლითონს შორის ყველაზე მაღალია, ამიტომაც კადმიუმს ზოგჯერ გამოიყენებენ კრიოგენული ტექნიკისათვის.
ფიზიოლოგიური ქმედება

კადმიუმის ნაერთები საწამლავია. განსაკუთრებულად საშიშია მისი ოქსიდის ორთქლის შესუნთქვა (CdO). ჰაერის შესუნთქვა 1 წთ-ის განმავლობაში რომელიც შეიცავს კადმიუმის ოქსიდს 2,5 გრ/მ3, ან 30 წმ-ის განმავლობაში სადაც კონცენტრაციაა 5 გრ/მ3 წარმოადგენს მომაკვდინებელს. კადმიუმი წარმოადგენს კანცეროგენს.
პირველადი დახმარება მწვავე კადმიუმით მოწამვლისას არის სუფთა ჰაერი, სრული სიმშვიდე, გაცივების თავიდან აცილება. სასუნთქი გზების გაღიზიანებისას — თბილი რძე სოდით, ინჰალაცია 2 %-იანი NaHCO3-ის სხნარით. ძლიერი ხველებისას — კოდეინი, დიონინი, მდოგვის საფენები მკერდზე, საჭიროა ექიმის დახმარება. კადმიუმის მარილებით მოწამვლისას მის ანტიდოტს წარმოადგენს ალბუმინი ნატრიუმის კარბონატთან.
მწვავე ტოქსიკურობა
კადმიუმის და ყველა მისი ნაერთის ორთქლი ტოქსიკურია, რაც დაკავშირებულია, კერძოდ, მის თვისებასთან დააკავშიროს გოგირდშემცველი ფერმენტები და ამინომჟავები.
კადმიუმის მარილებით მწვავე მოწამვლის სიმტომებია — ღებინება და კრუნჩხვები.
ქრონიკული ტოქსიკურობა
კადმიუმი — კუმულატიური საწამლავია (აქვს თვისება ორგანიზმში დაგროვებისა).
სანიტარულ-ეკოლოგიური ნორმატივები
სასმელ წყალში კადმიუმის ზღვრული დასაშვები კონცენტრაციაა 0,001 მგრ/დმ³ (СанПиН 2.1.4.1074-01).
ტოქსიკური ზემოქმედების მექანიზმი
კადმიუმის ტოქსიკური ზემოქმედების მექანიზმი ალბათ მდგომარეობს, კარბოქსილების, ამინების და განსაკუთრებულად ცილების მოლეკულების სულფჰიდრიდული ჯგუფების შეკავშირებასთან, რის შედეგად ქვეითდება ფერმენტული სისტემების აქტივობა. კადმიუმის ხსნადი ნაერთები სისხლში მოხვედრის შემდეგ აავადდება ცენტრალური ნერვიული სისტემა, ღვიძლი და თირკმლები, ირღვევა ფოსფორ-კალციუმის მიმოცვლა. ქრონიკული მოწამლვა იწვევს ანემიას და ძვლების დაშლას.
კადმიუმი ნორმალური, მცირე რაოდენობით არის ჯანმრთელი ადამიანის ორგანიზმში. კადმიუმი ადვილად გროვდება მზარდ უჯრედებში (მაგალითად სიმსივნის ან სასქესო). ის უკავშირდება უჯრედების ციტოპლაზმატურ და ბირთვულ მასალას და აზიანებს მას. ის ცვლის ჰორმონებისა და ფერმენტების აქტიურობას. ეს განპირობებულია მისი თვისებით დააკავშიროს სულფჰიდრილური (-SH) ჯგუფები.
იზოტოპები
კადმიუმის არსებული რვა ბუნებრივი იზოტოპიდან ექვსი სტაბილურია, ორ იზოტოპზე აღმოჩენილია რადიოაქტიურობა. ესენია 113Cd (იზოთოპური გავრცობადობა 12,22 %, ბეტა-დაშლა ნახევარდაშლის პერიოდით 7,7×1015 წელი) და 116Cd (იზოთოპური გავრცობადობა 7,49 %, ორმაგი ბეტა-დაშლა ნახევარდაშლის პერიოდით 3,0×1019 წელი).
იხ.ვიდეო - Кадмий 48. Жёлтый яд вокруг нас.
რეგულაციები
კადმიუმის მავნე ზემოქმედების გამო გარემოზე და ადამიანის ჯანმრთელობაზე, კადმიუმის მიწოდება და გამოყენება შეზღუდულია ევროპაში REACH რეგულაციის მიხედვით.
EFSA-ს პანელი კვების ჯაჭვში დამაბინძურებლების შესახებ განსაზღვრავს, რომ 2,5 მკგ/კგ სხეულის წონა არის ტოლერანტული ყოველკვირეული მიღება ადამიანებისთვის. FAO/WHO-ს გაერთიანებულმა საექსპერტო კომიტეტმა სურსათის დანამატებზე გამოაცხადა 7 მკგ/კგ სხეულის მასაზე, როგორც დროებითი ტოლერანტული ყოველკვირეული მიღება. კალიფორნიის შტატი მოითხოვს საკვების ეტიკეტს, რომელიც შეიცავს გაფრთხილებას კადმიუმის პოტენციური ზემოქმედების შესახებ ისეთ პროდუქტებზე, როგორიცაა კაკაოს ფხვნილი. ევროკომისიამ შემოიღო ევროკავშირის რეგულაცია (2019/1009) სასუქის პროდუქტების შესახებ (EU, 2019), მიღებული 2019 წლის ივნისში და სრულად გამოიყენება 2022 წლის ივლისიდან, ადგენს Cd-ის ზღვრულ მნიშვნელობას ფოსფატულ სასუქებში 60 მგ კგ-1-მდე. P2O5-დან.
აშშ-ის შრომის უსაფრთხოებისა და ჯანმრთელობის ადმინისტრაციამ (OSHA) დაადგინა კადმიუმის დასაშვები ექსპოზიციის ლიმიტი (PEL) დროში შეწონილი საშუალოდ (TWA) 0,005 ppm. შრომის უსაფრთხოებისა და ჯანმრთელობის ეროვნულმა ინსტიტუტმა (NIOSH) არ დააწესა ექსპოზიციის რეკომენდირებული ლიმიტი (REL) და დაასახელა კადმიუმი, როგორც ადამიანის ცნობილ კანცეროგენად. IDLH (სიცოცხლისა და ჯანმრთელობისთვის დაუყოვნებლივ საშიში) დონე კადმიუმისთვის არის 9 მგ/მ3.
| ლეტალური დოზა | ორგანიზმი | მარშრუტი | დრო |
|---|---|---|---|
| LD50: 225 mg/kg | ვირთხა | ორალური | n/a |
| LD50: 890 mg/kg | თაგვი | ორალური | n/a |
| LC50: 25 mg/m3 | ვირთხა | ჰაერიდან | 30 min |
ვერცხლისწყლის გარდა, ზოგიერთ ბატარეაში კადმიუმის არსებობამ გამოიწვია ბატარეების სათანადო განკარგვის (ან გადამუშავების) მოთხოვნა.
პროდუქტის გახსენება
2006 წლის მაისში, არსენალის საფეხბურთო კლუბის ძველი სტადიონიდან, ჰაიბერი, ლონდონში, ინგლისი, ადგილების გაყიდვა გაუქმდა, როდესაც სკამებში აღმოაჩინეს კადმიუმის კვალი. 2010 წელს ბავშვთა სამკაულებში კადმიუმის გამოყენების მაღალი დონის შესახებ მოხსენებებმა გამოიწვია აშშ-ს სამომხმარებლო პროდუქტის უსაფრთხოების კომისიის გამოძიება. აშშ-ს CPSC-მ გამოსცა სპეციალური შეტყობინებები კადმიუმის შემცველობის შესახებ Claire's და Wal-Mart მაღაზიების მიერ გაყიდულ სამკაულებში.
2010 წლის ივნისში მაკდონალდსმა ნებაყოფლობით გაიხსენა 12 მილიონზე მეტი სარეკლამო Shrek Forever After 3D კოლექციური სასმელის სათვალეები მინის ჭურჭელზე საღებავის პიგმენტებში კადმიუმის დონის გამო. სათვალეები დამზადებულია Arc International-ის მიერ, მილვილიდან, ნიუ ჯერსი, აშშ.
იხ.ვიდეო - Cadmium - cancer causing agent. sources and symptoms. Cadmium containing battery














