იონი
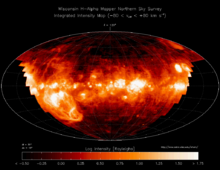
გავრცელება იონის წყაალბადის იონიზაცია ვარსკვლავთშორისო სივრცეში სხვადასხვა ნაწილში ჩვენ გალაქტიკაში გამოსახულია H-ალფა. დიაპაზოში
(ბერძნ. ion [i̯oːn] — მოსიარულე), ელექტრულად დამუხტული ატომებიან ატომთა ჯგუფები (მოლეკულები, რადიკალები და სხვა), რომლებიც წარმოიქმნება მათ მიერ ელექტრონების (ან სხვადასხვა დამუხტული ნაწილაკის) დაკარგვის ან შეძენის შედეგად. მაიკლ ფარადეიმ 1834 წელს, როდესაც იკვლევდა მჟავების, ტუტეებისა და მარილების წყალხსნარებზე ელექტრული დენის მოქმედებას, დაუშვა, რომ ასეთი წყალხსნარების ელექტროგამტარობა განპირობებულია იონების მოძრაობით. დადებითად დამუხტულ იონებს, რომლებიც ხსნარებში უარყოფითი პოლუსისაკენ (კათოდისაკენ) მოძრაობენ, ფარადეიმ კატიონები უწოდა, ხოლო უარყოფითად დამუხტულებს, რომლებიც დადებითი პოლუსისაკენ (ანოდისაკენ) მოძრაობენ, — ანიონები. ამის შესაბამისად იონების მუხტის ნიშანი ან დადებითია, ან უარყოფითი, მუხტის სიდიდე დამოკიდებულია ატომის მიერ დაკარგული ან შეძენილი ელექტრონების რაოდენობაზე. მაგ., Na+, Ca+, Al3+, Cl−, SO42−. იონები გვხვდება ნივთიერების ყველა აგრეგატულ მდგომარეობაში — აირებში, სითხეებში, კრისტალებში

იონები იყოფა ორ დიდ ჯგუფად - უბრალო და რთული
მარტივი (მონოატომური) იონი შეიცავს ერთ ატმის ბირთვს
რთული (პოლიატომური) იონი შეიცავს არა უმცირესს ორ ატმის ბირთვს
ცალკე გამოყოფენ იონ-რადიკალებს - დამუხტული თავისუფალი რადიკალები. იონი-რადიკალები თავის მხრივ ყოფენ ქვეკლასად კატონ-რადიკალად და ანიონ-რადიკალდ
კატიონ-რადიკალი - დადებითად დამუხტული ნაწილაკები ერთ არაწყვილი ელექტრონით
ანიონ-რადიკალი - უარყოფითად დამუხტული ნაწილაკი ერთი დაუწყვილებები ელექტრონით
სხვათაშორის იონები მნიშვნელოვან როლს ასრულებს ადამიანის ბიოფიზიკურ პროცესებზე.
იხ. ვიდეო
ეხლა გავაგრძელოთ და ვნახოთ რა არის ელექტრო ველი. მარტივი იონები შედგება ერთ ატომის ბირთვიდან და ელექტრონიდან. ატომის ბირთვი შედგება პროტონისგან და ნეიტრონისგან, ატარებენ მთელი (მეტი 99,8%) მასას იონისა და ქმნის დადბითი დამუხტული ელექტრონული ველს. ატომის მუხტი განისაზღვრება პროტონებით, რ-ემთხვევა მნდელეევის ცხრილის ელეემნტის ნომრებს (მიხვდით ალბათ ეს კი ქიმია არის)
ატომები და მოლეკულებს შეუძლიათ გადაქცევა დადებითად დამუხტული იონებად შედეგად ერთ და ორი რამდენიმე ელექტრონი. მოწყვეტა ელექტრონის სჭირდება ენერგიის დახარჯვა, რ-საც ენერგიის იონიზაცია ქვია
კავშირის ენერგიის ერთ-ერთი სახეობაა ან, როგორც მას ზოგჯერ უწოდებენ, პირველი იონიზაციის პოტენციალი (I1) (მრავალელექტრონიანი ატომისათვის არსებობს მეორე, მესამე და ა.შ. იონიზაციის პოტენციალები, რომლებიც წარმოადგენენ ელექტრონის მოცილების ენერგიას მისი თავისუფალი კათიონისაგანმუხტით +1, +2 და ა.შ. ეს იონიზაციის პოტენციალები, როგორც წესი, ნაკლებად მნიშვნელოვანია ქიმიური ელემენტის დასახასიათებლად), წარმოადგენს უმცირეს ენერგიას, რომელიც საჭიროა თავისუფალი ატომიდან ელექტრონის მოსაცილებლად, მის დაბალ ენერგეტიკულ (ძირითად) მდგომარეობიდან უსასრულობაში. იონიზაციის ენერგია წარმოადგენს ატომის ერთ-ერთ მთავარ მახასიათებელს, რომელზედაც მნიშვნელოვანწილად დამოკიდებულია ატომებს შორის შექმნილი ქიმიური კავშირის ბუნება და სიმტკიცე. ატომის იონიზაციის ენერგიისაგან მნიშვნელოვნადაა დამოკიდებული ასევე შესაბამისი მარტივი ნივთიერების აღმდგენი თვისებები. ატომის იონიზაციის ენერგიაზე არსებითი გავლენა აქვს შემდეგ ფაქტორებს:
იზ. ვიდეო
- ბირთვის ეფექტიანი მუხტი, რომელიც წარმოადგენს ატომში ელექტრონების რიცხვის ფუნქციას, ეკრანირირებს ბირთს და უფრი ღრმად მდებარე ორბიტალებზე;
- რადიალური მანძილი ბირთვიდან ელექტრონამდე რომელიც ატომის ბირთვათნ ყველაზე სუსტადაა დაკავშირებული და იონიზაციისას სტოვებს მას;
- ელექტრონის შეღწევადობის უნარის ზომა;
- გარე (ვალენტური) ელექტრონების, ელექტრონებსშორისი განზიდვა.

დამოკიდებული იონიზაციის ენერგია ატომის ნომრის ელემნტის რიგითობით
იონიზაცია
ფიზიკური პროცესი, რომლის დროსაც ატომებისა ან მოლეკულებისაგან წარმოიქმნება იონებიპროტონებისა და ელექტრონების რაოდენობის ცვლილებით.
იონიზაციის პროცესი ძირითადად ასოცირდება ნივთიერებიდან ელექტრონების ამოგლეჯით, რომლის დროსაც ბმულ მდგომარეობაში მყოფმა ელექტრონმა უნდა მიიღოს საკმარისი ენერგია რათა გადალახოს იონიზაციის პოტენციალი

ენერგია იონიზაციის სუფთა ქიმიური ელემენტები. პიკში მდგომარეობაში ინერტულ აიარში
იონიზაცია რომელიც განიხილება კლასიკური ფიზიკის ფარგლებში. ანუ იმისათვის, რომ ელექტრონი ამოგლეჯილ იქნას ატომიდან ან მოლეკულიდან, აუცილებელია სულ მცირე ენერგიის იმ რაოდენობის გადაცემა, რამდენიც საჭიროა მოცემული დონიდან ელექტრონის ამოსაგლეჯად.
იხ. ვიდეო





Комментариев нет:
Отправить комментарий